Кетен (химич.)
Большая Советская Энциклопедия. Статьи для написания рефератов, курсовых работ, научные статьи, биографии, очерки, аннотации, описания.
|
|
| КЕБ |
| КЕВ |
| КЕГ |
| КЕД |
| КЕЕ |
| КЕЗ |
| КЕЙ |
| КЕК |
| КЕЛ |
| КЕМ |
| КЕН |
| КЕП |
| КЕР |
| КЕС |
| КЕТ |
| КЕУ |
| КЕФ |
| КЕХ |
| КЕЦ |
| КЕЧ |
| КЕШ |
| КЕЭ |
Кетен, карбометилен, первый член ряда кетенов RR'C=C=O; ненасыщенное, очень реакционно-способное органическое соединение CH2=C=O Кетен (химич.) — газ, tkип — 41°С, tпл — 134,6°С. Кетен (химич.) — эффективный ацетилирующий агент; при действии на соединения с подвижным атомом водорода, например на спирты, тиолы, амины, кислоты, образуются продукты ацетилирования, например: ROH + CH2 = C = O ® ROCOCH3.
Кетен (химич.) легко присоединяет воду с образованием уксусной кислоты, а также кетоны; так, из Кетен (химич.) и ацетона получается диметил-b-пропиолактон 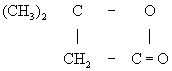
Кетен (химич.) устойчив при — 80°С, при 0°С он легко димеризуется в дикетен (метилен-b-пропиолактон) 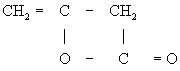
из которого пиролизом при 550—600°С можно регенерировать Кетен (химич.) По токсичности Кетен (химич.) близок к фосгену.
В промышленности Кетен (химич.) получают пиролизом уксусной кислоты в присутствии триэтилфосфата или пиролизом ацетона над глинозёмом. Общий метод синтеза Кетен (химич.) и др. кетенов состоит в отщеплении галогенов от галогенангидридов a-галогенкарбоновых кислот:
RRўCX — COX ® RRўC = C = O + ZnX2 (X — атом галогена).
В лаборатории Кетен (химич.) удобно получать пиролизом ацетона или уксусного ангидрида в специальном приборе — так называемой кетенной лампе.
Кетен (химич.) применяют в промышленности для превращения уксусной кислоты в ангидрид, для получения ацетилцеллюлозы, в синтезе пропиолактона и др.
Лит.: Лейси Р. Н., Кетен в органическом синтезе, в кн.: Успехи органической химии, пер. с англ., т. 2, М., 1964, с. 204.
Я. Ф. Комиссаров.
|
Так же Вы можете узнать о... Дрёма (Melandrium), род растений семейства гвоздичных. Железный шпат, то же, что сидерит. Звёздное время, система счёта времени, в основе которой лежат звёздные сутки; применяется при различных астрономических наблюдениях. Ижевский Василий Петрович [4(16).6.1863, Рязань, — 23. «Иомиури», «Иомиури симбун», одна из крупнейших буржуазных газет в Японии. Калан, морская выдра, камчатский бобр (Enhydra lutris), хищное млекопитающее семейства куньих. Кариес зубов, поражение твёрдых тканей зуба, выражающееся в последовательном его разрушении (эмали, дентина, цемента) с образованием полости. Керамические краски, окрашенные минеральные вещества, стойкие при высоких температурах, применяемые для окраски керамических изделий, глазурей и стекол. «Книжная летопись», библиографический журнал, орган государственной библиографии СССР. Комптоновская длина волны, величина размерности длины, характерная для релятивистских квантовых процессов; выражается через массу частицы т и универсальные постоянные h и с (h — Планка постоянная, с — скорость света): l0 = h/mc. Корякское нагорье, Корякский хребет, нагорье на северо-востоке Азиатской части СССР, в Камчатской и Магаданской области РСФСР. Крозе острова (Crozet), группа скалистых вулканических островов в Индийском секторе Южного океана (46° южной широты и 50—52° восточной долготы). Кызыл-Ирмак (тур. Kizilirmak — красная река; античное название — Галис), река в Турции. Ленарт Йозеф Ленарт (Lenart) Йозеф (р.3.4.1923, Липтовска-Порубка), государственный и политический деятель ЧССР. Лихтенштадт Владимир Осипович (16.12.1882 — 15. |
|