Бензол
Большая Советская Энциклопедия. Статьи для написания рефератов, курсовых работ, научные статьи, биографии, очерки, аннотации, описания.
|
|
| БЕА |
| БЕБ |
| БЕВ |
| БЕГ |
| БЕД |
| БЕЕ |
| БЕЖ |
| БЕЗ |
| БЕЙ |
| БЕК |
| БЕЛ |
| БЕМ |
| БЕН |
| БЕО |
| БЕП |
| БЕР |
| БЕС |
| БЕТ |
| БЕХ |
| БЕЦ |
| БЕЧ |
| БЕШ |
| БЕЩ |
| БЕЭ |
| БЕЯ |
Бензол.
Бензол, органическое соединение C6H6, простейший ароматический углеводород; подвижная бесцветная летучая жидкость со своеобразным нерезким запахом; tnл 5,5°C; tkип 80,1°С; плотность 879,1 кг [м3 (0,8791 г/см3) при 20°С; n20D 1,5011. С воздухом в объёмной концентрации 1,5—8% Бензол образует взрывоопасные смеси. Бензол смешивается во всех соотношениях с эфиром, бензином и др. органическими растворителями; в 100 г Бензол при 26°С растворяется 0,054 г воды; с водой образует азеотропную (постоянно кипящую) смесь (91,2% Бензол по массе) с tkип 69,25°С.
Бензол.
Бензол открыт М. Фарадеем. (1825), который выделил его из жидкого конденсата светильного газа; в чистом виде Бензол получен в 1833 Э. Мичерлихом, сухой перегонкой кальциевой соли бензойной кислоты (отсюда название).
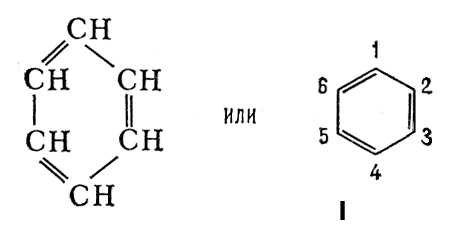
В 1865 Ф. А. Кекуле предложил для Бензол формулу строения I, соответствующую циклогексатриену — замкнутую цепь из 6 атомов углерода с чередующимися простыми и двойными связями. Формулой Кекуле довольно широко пользуются, хотя накоплено много фактов, свидетельствующих о том, что Бензол не обладает строением циклогексатриена. Так, давно установлено, что орто-дизамещённые Бензол (например, 1,2 и 1,6) существуют лишь в одной форме, тогда как формула Кекуле допускает изомерию таких соединений (заместители у атомов углерода, связанных простой или двойной связью). В 1872 Кекуле дополнительно ввёл гипотезу о том, что связи в Бензол постоянно и очень быстро перемещаются, осциллируют. Были предложены и др. формулы строения Бензол, однако они не получили признания. 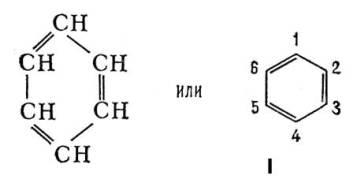
Химические свойства Бензол формально в некоторой степени соответствуют формуле (1). Так, в определённых условиях к молекуле Бензол присоединяются 3 молекулы хлора или 3 молекулы водорода; Бензол образуется при конденсации 3 молекул ацетилена. Однако для Бензол характерны в основном не реакции присоединения, типичные для ненасыщенных соединений, а реакции электрофильного замещения. Кроме того, бензольное ядро очень устойчиво к действию окислителей, например перманганата калия, что также противоречит наличию в Бензол локализованных двойных связей. Особые, т. н. ароматические, свойства Бензол объясняются тем, что все связи в его молекуле выравнены, т. е. расстояния между соседними атомами углерода одинаковы и равны 0,14 нм (1,40 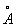 ), длина простой связи С—С 0,154 нм (1,54
), длина простой связи С—С 0,154 нм (1,54 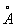 ) и двойной С = С 0,132 нм (1,32
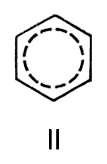
) и двойной С = С 0,132 нм (1,32 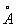 ). Молекула Бензол имеет ось симметрии шестого порядка; для Бензол как ароматического соединения характерно наличие секстета p-электронов, образующих единую замкнутую устойчивую электронную систему. Однако до сих пор нет общепринятой формулы, отражающей его строение; часто используют формулу II.
). Молекула Бензол имеет ось симметрии шестого порядка; для Бензол как ароматического соединения характерно наличие секстета p-электронов, образующих единую замкнутую устойчивую электронную систему. Однако до сих пор нет общепринятой формулы, отражающей его строение; часто используют формулу II. 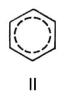
Бензол содержится в продуктах сухой перегонки каменного угля (коксовом газе) и небольшое количество — в коксовой смоле. Значительные количества Бензол получают также каталитической циклизацией алифатических углеводородов нефти (см. Ароматизация нефтепродуктов). Бензол — важнейшее сырьё химической промышленности. При действии азотной кислоты на Бензол образуется нитробензол С6Н5NО2, который может быть восстановлен в анилин C6H5NH2 — исходный продукт в производстве многих красителей. При взаимодействии Бензол с серной кислотой получается бензолсульфокислота C6H5SO2OH, щелочное плавление солей которой — один из основных методов производства фенола. При алкилировании Бензол этиленом в присутствии хлористого алюминия получается этилбензол, каталитическое дегидрирование которого представляет собой основной способ производства стирола C6H5CH=CH2. Аналогично из Бензол и пропилена образуется изопропилбензол C6H5CH (CH3)2 — исходный продукт для получения фенола и ацетона в промышленном масштабе. Широко применяют и галогенопроизводные Бензол Так, хлорбензол омыляется в фенол; из хлорбензола и магния Гриньяра реакцией получают фенилмагнийхлорид C6H5MgCI, при реакции которого с окисью этилена образуется b-фенилэтиловый спирт C6H5CH2CH2OH, используемый в парфюмерии как искусственное розовое масло. При каталитическом гидрировании Бензол превращается в циклогексан — исходный продукт в одном из способов производства капролактама, полимеризацией которого получают синтетическое волокно «капрон». При облучении Бензол присоединяет 3 моля хлора с образованием смеси стереоизомерных гексахлорциклогексанов, один из которых (гексахлоран) обладает сильными инсектицидными свойствами. Бензол применяют в производстве взрывчатых веществ, а также как растворитель и экстрагирующее средство в производстве лаков, красок и др.
Лит.: Неницеску К. Д., Органическая химия, пер. с рум., т. 1, М., 1962, с. 304, 323.
Я. Ф. Комиссаров.
Действие на организм. Бензол может вызывать острые и хронические отравления. Проникает в организм главным образом через органы дыхания, может всасываться и через неповрежденную кожу. Предельно допустимая концентрация паров Бензол в воздухе рабочих помещений 20 мг/м3. Выводится через лёгкие и с мочой. Острые отравления происходят обычно при авариях; их наиболее характерные признаки: головная боль, головокружение, тошнота, рвота, возбуждение, сменяющееся угнетённым состоянием, частый пульс, падение кровяного давления, в тяжёлых случаях — судороги, потеря сознания. Хроническое отравление Бензол проявляется изменением крови (нарушение функции костного мозга), головокружением, общей слабостью, расстройством сна, быстрой утомляемостью; у женщин — нарушением менструальной функции. Надёжная мера против отравлений парами Бензол — хорошая вентиляция производственных помещений.
Лечение при острых отравлениях: покой, тепло, бромистые препараты, сердечно-сосудистые средства; при хронических отравлениях с выраженной анемией: переливание эритроцитарной массы, витамин B12, препараты железа.
Лит.: Омельяненко Л. М. и Сенкевич Н. А., Клиника и профилактика отравлений бензолом, М., 1957; Профессиональные болезни, 2 изд., М., 1964.
|
Так же Вы можете узнать о... Гнесина Елена Фабиановна [18(30).5.1874, Ростов-на-Дону, — 4. Диалектика [греч. dialektike (technе) — искусство вести беседу, спор, от dialegomai — веду беседу, спор], учение о наиболее общих закономерностях становления, развития, внутренний источник которых усматривается в единстве и борьбе противоположностей. Зенитный артиллерийский комплекс (ЗАК), зенитное оружие, представляющее собой совокупность одной или нескольких зенитных пушек, прибора управления артиллерийским зенитным огнем (ПУАЗО) и радиолокатора. Кантабры (лат. Cantabri), одно из иберийских племён в Северной Испании. Компаратор интерференционный, прибор для метрологических измерений длин мер в длинах волн света или для сравнения длин мер на основе интерференции света. Лазы, чаны, этнографическая группа грузин, в прошлом одно из грузинских племён. Мамедкулизаде Джалил (псевдоним — Молла Насреддин) (22. Мориц Саксонский (Maurice de Saxe) (28.10.1696, Гослар, — 30. Обезволашивание, удаление волосяного покрова со шкуры при переработке ее на кожу. Первый съезд Советов СССР, съезд Советов рабочих, крестьянских и красноармейских депутатов, провозгласивший образование первого в мире многонационального социалистического государства — Союза Советских Социалистических Республик. Принсепия (Prinsepia), род листопадных колючих кустарников семейства розоцветных. |
|