Валентность (химич.) 2. Эволюция понятия «валентность» и его роль в истории химии
Большая Советская Энциклопедия. Статьи для написания рефератов, курсовых работ, научные статьи, биографии, очерки, аннотации, описания.
|
|
| ВАА |
| ВАБ |
| ВАВ |
| ВАГ |
| ВАД |
| ВАЕ |
| ВАЖ |
| ВАЗ |
| ВАИ |
| ВАЙ |
| ВАК |
| ВАЛ |
| ВАМ |
| ВАН |
| ВАП |
| ВАР |
| ВАС |
| ВАТ |
| ВАУ |
| ВАФ |
| ВАХ |
| ВАЦ |
| ВАЧ |
| ВАШ |
| ВАЩ |
| ВАЯ |
2. Эволюция понятия «валентность» и его роль в истории химии
В начале 19 в. Дж. Дальтоном был сформулирован закон кратных отношений, из которого следовало, что каждый атом одного элемента может соединяться с одним, двумя, тремя и т.д. атомами другого элемента (как, например, в окислах азота —N2O, NO, N2O3, NO2 и N2O5). В середине 19 в., когда были определены точные относительные веса атомов (И. Я. Берцелиус и др.), стало ясно, что наибольшее число атомов, с которыми может соединяться данный атом, не превышает определённой величины, зависящей от его природы. Например, атом F может соединяться лишь с одним атомом Н, О — с двумя, N — с тремя, С — с четырьмя, образуя соответственно HF, H2O, NH3 и CH4. Два или четыре атома Н в метане CH4 могут быть замещены одним или двумя атомами О с образованием формальдегида CH2O и двуокиси углерода CO2 соответственно, три атома Н в CH4 могут замещаться одним атомом N с образованием цианистого водорода HCN, и т.д. Эта способность связывать или замещать определённое число других атомов и была названа «Валентность (химич.)» (Э. Франкленд, 1853).
В таком определении Валентность (химич.), естественно, всегда выражается целыми числами. Поскольку в то время для водорода не были известны соединения, где он был бы связан более чем с одним атомом любого другого элемента, атом Н был выбран в качестве стандарта, обладающего Валентность (химич.), равной 1. В «водородной» шкале кислород и сера имеют Валентность (химич.), равную 2, азот и фосфор 3, углерод и кремний 4. Однако «водородной» шкалы оказалось недостаточно: в других соединениях, например в окислах, один и тот же элемент может реализовать Валентность (химич.), которые не осуществляются в гидридах (существуют окислы P2O5, SO3 и Cl2O7, но неизвестны гидриды PH5, SH6 и ClH7). В качестве второго стандарта с Валентность (химич.), равной 2, был выбран кислород.
В конце 50-х гг. 19 в. А. С. Купер и А.Кекуле постулировали принцип постоянной четырёхвалентности углерода в органических соединениях. Представления о Валентность (химич.) составили важную часть теории химического строения А. М. Бутлерова (1861) (см. Химического строения теория). Образование химической связи рассматривалось как результат взаимного насыщения двух Валентность (химич.) пары взаимодействующих атомов (по одной Валентность (химич.) от каждого), кратные связи соответствовали насыщению нескольких Валентность (химич.) от каждого атома, и т.д. Каждая связь считалась локализованной между двумя атомами и изображалась одной чертой, соединяющей эти атомы. Молекулы стали изображать с помощью структурных формул, получивших особенно широкое распространение в органической химии.
Положения Бутлерова в дальнейшем легли в основу структурной теории, рассматривающей и пространственное расположение атомов в молекуле. Было найдено, что простые молекулы типа MXk с одинаковым центральным атомом M и разными заместителями Х имеют схожее геометрическое строение. Независимость геометрического строения от типа связи в широких пределах привела к мысли, что пространственное расположение атомов в молекулах MXk определяется Валентность (химич.) центрального атома М и что эти Валентность (химич.) имеют направленный характер (см. раздел 3).
Периодический закон Д. И. Менделеева (1869) вскрыл зависимость Валентность (химич.) элемента от его положения в периодической системе (см. Периодическая система элементов Д. И. Менделеева). Элементы одинаковых групп системы обладают одинаковой высшей Валентность (химич.), в большинстве случаев равной номеру той группы, в которой находится этот элемент; высшая Валентность (химич.) меняется на 1 при переходе от одной группы к соседним. Эта зависимость сыграла чрезвычайно важную роль в развитии химии: зная лишь положение элемента (в том числе элементов, которые в то время ещё не были открыты) в периодической системе, можно было определить его валентные возможности, предсказать состав его соединений и впоследствии синтезировать их. С помощью представлений о формальной (стехиометрической) Валентность (химич.) (см. Стехиометрия) химикам удалось обобщить и систематизировать огромный экспериментальный материал по строению, стехиометрическому составу и свойствам многих десятков и сотен тысяч органических и неорганических соединений.
Первые электронные теории ковалентности и гетеровалентности. До электронных представлений о строении вещества Валентность (химич.) трактовалась формально. Лишь в 20 в. было установлено, что химическая связь осуществляется за счёт электронов внешних (валентных) оболочек атомов.
В 1916 Г. Льюис постулировал, что химическая связь осуществляется парой электронов, принадлежащих одновременно обоим взаимодействующим атомам. В 1917 Валентность (химич.) Коссель выдвинул гипотезу, согласно которой электронная пара связи переходит целиком к одному из атомов с образованием ионной пары катион — анион, удерживающихся в молекуле электростатическими силами. Согласно обеим гипотезам наиболее устойчивыми оказываются соединения, в которых валентные электроны распределялись так, чтобы каждый атом был окружен оболочкой, имитирующей электронную оболочку ближайшего инертного газа (правило октета). Гипотеза Льюиса положила начало электронной теории ковалентной связи и ковалентности, гипотеза Косселя — теории ионной связи и гетеровалентности. Обе представляли крайние случаи общей картины полярной связи, когда электронная пара смещена к одному из атомов лишь частично и степень смещения может варьировать от 0 до 1 (см. Полярность химических связей). Валентность (химич.) атома в соединении, согласно классической электронной теории, равна числу его неспаренных электронов, участвующих в связях, а максимальная Валентность (химич.) — обычно полному числу электронов в его валентной оболочке, то есть номеру труппы периодической системы, в которой находится элемент. Элементы одинаковых групп имеют одинаковое число валентных электронов, а внутри одинаковых подгрупп — и одинаковые или очень близкие электронные конфигурации (см. раздел 3). Сходство строения валентных оболочек атомов обусловливает сходство их соединений.
Ковалентность и гетеровалентность отражают специфику соответствующего типа химической связи. Для ковалентности важна насыщаемость связей, обусловливающая существование молекул в виде дискретных частиц с определённым составом и структурой. Ковалентность эффективна для органических и большинства простых неорганических соединений. Напротив, в случае гетеровалентности максимальное число ионов противоположного знака, способное разместиться вокруг данного иона, в основном определяется соотношениями их размеров. Ионная Валентность (химич.) эффективна для сравнительно ограниченного класса соединений, в основном для различных солей щелочных, щёлочноземельных и некоторых др. металлов.
Валентность (химич.) в комплексных соединениях. Ещё в конце прошлого века было найдено (А. Вернер, 1893), что многие соединения, как с максимальными (насыщенновалентные), так и с промежуточными Валентность (химич.), типа ВСl3, SiCl4, PCl5, CrCl3 и т.п., обладают склонностью к взаимодействию с другими насыщенновалентными соединениями — солями, окислами, молекулами типа H2O, NH3 и др., с образованием довольно прочных комплексных соединений — K [BCl4], K2[SiCl6], NH4[PCl6] и т.д. Исследования их строения рентгеновскими методами показали, что в комплексных анионах 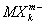 и катионах
и катионах 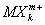 атомы лигандов Х обычно находятся в вершинах правильных многоугольников (октаэдра, тетраэдра и др.), а все связи М — Х одинаковы.
атомы лигандов Х обычно находятся в вершинах правильных многоугольников (октаэдра, тетраэдра и др.), а все связи М — Х одинаковы.
Для представлений о Валентность (химич.) комплексные соединения необычны тем, что в них координационное число КЧ может быть больше общего числа валентных электронов атома М. Более того, в парамагнитных (см. Магнетохимия) комплексах переходных и редкоземельных металлов — K4[CrF6], K3[CrF6], K2[CrF6] и др., некоторые электроны валентной оболочки остаются неспаренными и локализованными у центрального атома и практически не участвуют в связи. Классическая Валентность (химич.) и КЧ, как правило, не совпадают, а способность к образованию октаэдрических и тетраэдрических. комплексов оказалась чрезвычайно распространённой и типичной для многих металлов и неметаллов, связанной сложной зависимостью с положением элемента в периодической системе и его Валентность (химич.) в исходном простом соединении.
Поэтому было высказано предположение, что, наряду с «классической» Валентность (химич.), которая реализуется в исходных простых соединениях типа ВСl3, SiCl4 и др., атомы обладают также «координационной» Валентность (химич.) (см. Донорно-акцепторная связь), которая насыщается в комплексных соединениях (о природе координационной Валентность (химич.) см. раздел 3). Предпринимались попытки описать связь в комплексных соединениях в рамках ионной теории, в которой считается, что анионы типа [PF6]- и [МnO4]- построены из ионов P5+ + 6F- и Mn7+ + 4O2- и что Валентность (химич.) центрального атома совпадает с зарядом его иона. Однако затраты энергии, необходимой для перевода 1 атома Mn и 4 атомов О в состояния Mn7+ и O2-, далеко не компенсируются выигрышем в энергии при образовании связи. С появлением экспериментальных методов определения эффективных зарядов стало ясно, что эффективные заряды вообще редко превышают значения +1 или +2 у положительно заряженных и —1 у отрицательно заряженных атомов и обычно выражаются дробными долями заряда электрона (в перманганатном анионе заряд на Mn составляет лишь +1,5—+2,0 электрона). Поэтому ионная теория для большинства неорганических соединений, простых и комплексных, не может считаться корректной.
Успехи химии 20 в. и проблемы теории Валентность (химич.) В 20 в. экспериментальной химией было синтезировано и изучено строение множества новых соединений, которые также оказалось невозможно уместить в рамки классических представлений о Валентность (химич.) Оказалось, что склонность к образованию координационных соединений и насыщению координационных Валентность (химич.) вообще чрезвычайно распространена и характерна практически для всех элементов и что суждения о Валентность (химич.) на основании одного лишь стехиометрического состава очень часто оказываются несостоятельными без точных данных о структуре соединения и геометрическом расположении ближайшего окружения рассматриваемого атома. По мере развития структурных методов (см. Электронография молекул, Рентгенография молекул) стало известно, что многие соединения с простым брутто-составом (AlCl3, PdCl2, MoO3 и др.), ранее считавшиеся простыми, в действительности даже в парах имеют димерное и полимерное строение — Al2Cl6, (PdCl2) x (рис. 1, а, б), (MoO3)2-5. В них «мостиковые» лиганды, соединённые одинаковыми связями с двумя атомами металлов (на рис. 1 они помечены цифрой 2), обладают координационным числом КЧ = 2. У соединений в твёрдом состоянии, которые часто построены ещё сложнее, КЧ галогенов и кислорода, ранее выбранного в качестве стандартного двухвалентного элемента, могут быть 3 и даже 4. В бороводородах каждый «мостиковый» атом водорода, считавшегося ранее стандартным одновалентным элементом, связан одинаковыми связями с двумя атомами бора (рис. 1, б). Алкильные группы также способны образовывать мостиковые связи в металлоорганических соединениях типа Al2(CH3)6 (рис. 1, г) и др.
Рис. 1. Мостиковые лиганды (Cl, H, CH3) в димерных и полимерных соединениях: Al2Cl6 (а), (PdCl2)x (б), В2Н6 (в) и Al2(CH3)6 (г).
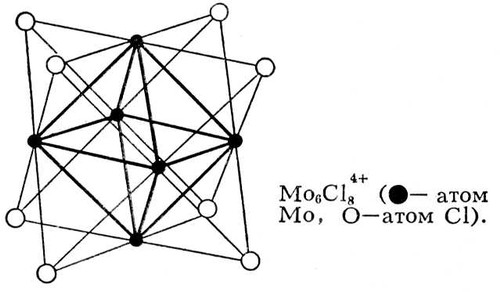
Для соединений переходных и ряда непереходных элементов оказалось характерным использование дополнительной Валентность (химич.) за счёт образования связей металл — металл (кластерные соединения), при этом расстояние между атомами металлов оказалось значительно меньшим, чем в индивидуальных металлах. Например, в дигалогенидах молибдена и вольфрама во многих химических реакциях сохраняется неизменной группа 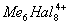 (рис. 2), в которой атомы металла (Me) образуют правильный октаэдр; каждый атом Me связан с четырьмя другими атомами Me и с четырьмя атомами галогена (Hal), а каждый атом Hal связан с тремя атомами Me. Связи Me — Me в кластерах могут быть кратными (как, например, в
(рис. 2), в которой атомы металла (Me) образуют правильный октаэдр; каждый атом Me связан с четырьмя другими атомами Me и с четырьмя атомами галогена (Hal), а каждый атом Hal связан с тремя атомами Me. Связи Me — Me в кластерах могут быть кратными (как, например, в 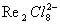 , где расстояние Re — Re на 0,5
, где расстояние Re — Re на 0,5 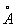 меньше, чем в металлическом Re, и на их образование атомы могут тратить не одну, а несколько Валентность (химич.)
меньше, чем в металлическом Re, и на их образование атомы могут тратить не одну, а несколько Валентность (химич.)
Рис. 2. Кластерная структура Mo6Cl4+8 ( — атом Mo,
— атом Mo,  — атом Cl).
— атом Cl).
Недостаточность классического понимания Валентность (химич.) видна также на примере так называемых «нуль-валентных» соединений, где атом металла связан исключительно с нейтральными молекулами; таковы карбонилы металлов типа Ti (CO)7, Cr (CO)6, Fe (CO)5, аммиакаты типа Pt (NH3)4 и т.д. В них вообще отсутствует классическое валентное взаимодействие (у атомов С и N в молекулах CO и NH3 нет неспаренных электронов), а связь осуществляется только за счёт координационных Валентность (химич.) атома металла и молекул лигандов. Нейтральные лиганды часто оказываются мостиковыми и образуют по две, например в Co4(CO)12, и даже по три, например в Rh6(CO)16, связи.
Для теории Валентность (химич.) особый интерес представляют так называемые p-комплексы переходных металлов с ароматическими молекулами или молекулами с сопряжёнными связями в качестве лигандов (этиленом, циклопентадиенилом, бензолом и др.) типа ферроцена Fe (C5H5)2, дибензолхрома Cr (C6H6)2 (рис. 3, а, б), тетрациклопентадиенила титана Ti (C5H5)4 и др. В отличие от комплексов типа [Сr (NHз)6]3+, [Сr (H2O)6]2+ или Cr (CO)6, где центральный атом осуществляет связь с лигандом через один атом от каждого лиганда (через N — в аммиакатах, через О — в гидратах, и т.д.), в p-комплексах атомы Fe, Cr и Ti взаимодействуют совершенно одинаково со всеми атомами С каждого ароматического кольца. Непригодность классической Валентность (химич.) или КЧ здесь очевидна: при этом пришлось бы считать все атомы углерода 5-валентными, а атомы Fe, Cr и Ti — соответственно 10-, 12и 20-валентными. Единственный неспаренный электрон, который имеется у радикала ×C5H5 (так же как и у многих других ароматических радикалов типа тропила ×C7H7 и т.д.), в равной степени принадлежит всем углеродным атомам кольца. Для этого класса соединений потребовались представления о делокализованной («групповой») Валентность (химич.), характеризующей всю совокупность атомов С в ароматическом кольце.
Рис. 3. (p-Комплексы переходных металлов ( — атом металла,
— атом металла, 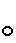 — атом С): ферроцен Fe(C5H5)2 (а), дибензолхром Cr(C6H6)2 (б).
— атом С): ферроцен Fe(C5H5)2 (а), дибензолхром Cr(C6H6)2 (б).
Сейчас стало ясно, что КЧ в комплексах, так же как Валентность (химич.) в простых соединениях, не является жестко специфической характеристикой элемента: для большого числа металлов были найдены комплексы со всеми промежуточными значениями КЧ от 3 до 7, 8 и 9. При этом возникли трудности с самим определением КЧ: в низкосимметричных высококоординационных комплексах расстояния М — Х, даже для одинаковых лигандов X, часто оказываются неодинаковыми; при этом они могут быть больше тех достаточно коротких расстояний, при которых наличие сильного взаимодействия бесспорно, но всё же недостаточно велики, чтобы их можно было уверенно исключить из координационной сферы комплекса.
Новые проблемы Валентность (химич.) возникли и в других разделах химии. Сильное развитие получила химия свободных радикалов [например, метил ×CH3, трифенилметил ×C (C6H5)3 и др., см. Радикалы свободные], в которых имеются атомы 3-валентного углерода. В последнем десятилетии были синтезированы соединения инертных газов типа XeF2, XeF4, XeF6, XeO3 и др., то есть соединения элементов, которые ранее считались вообще неспособными к химическому взаимодействию. Стало ясно и то, что Валентность (химич.) элементов может сильно меняться с изменением внешних условий, в частности температуры. Например, PCl5, существующий при умеренных температурах в газовой фазе в виде мономерных молекул, при конденсации диспропорционирует (см. Диспропорционирования реакция), давая пару катион [РСl4]+ (КЧ = 4) — анион [РСl6]- (КЧ = 6). Наоборот, при повышении температуры обнаруживаются молекулы PCl3, PCl2, PCl, ионы PCl4+, PCl3+, Pd2+, PCl+ и т.д. Благодаря успехам химии молекул в газовой фазе за последние 20 лет найдено огромное число соединений (часто сложного состава) с промежуточными и необычными Валентность (химич.), которые не обнаруживаются у соединений в обычных условиях. Например, кроме давно известных анионов типа CO32- и SO42-, сейчас обнаружены анионы CO3-, SO4- и нейтральные молекулы CO3, SO4. Кроме насыщенных молекул типа CH4, C2H6, найдены ионы типа CH5+, C2H7+, кроме молекулы H2 — ион Нз+, и т.д.
Сейчас установлено, что подавляющее большинство элементов может проявлять переменную Валентность (химич.), образуя весь ряд «валентноненасыщенных» соединений со всеми значениями Валентность (химич.) от 1 до максимальной с изменением на 1 (например, известны молекулы BF, BF2 и BF3; CF, CF2, CF3 и CF4 и т.д.). Валентность (химич.) не может считаться жестко специфической характеристикой элемента, можно говорить лишь об относительной типичности или относительной устойчивости разных значений Валентность (химич.) У непереходных элементов чётных и нечётных групп наиболее устойчивы соответственно чётные и нечётные Валентность (химич.), например в молекулах типа PF3, PF5, SF2, SF4, SF6, IF, IF3, IF5, IF7 и т.д., где типичная Валентность (химич.) атомов Р, S и I изменяется на 2 единицы.
Радикалы типа ·PF4, ·SF3, ·SF5, ·IF2, ·IF4 и т.д. с четырёхвалентным фосфором, нечётновалентными аналогами серы и инертными газами и чётновалентными галогенами значительно менее стабильны, обладают отчётливо выраженной склонностью к отщеплению одного электрона (с образованием более устойчивых катионов типа PF4+, SF3+, SF5+, IF2+, IF4+) или одного атома заместителя и характеризуются значительно меньшими временами существования. У элементов побочных групп соотношения между типичными и менее типичными Валентность (химич.) имеют более сложный характер.
Изучение электронных спектров показало, что двухатомные молекулы типа O2, S2, OS и др. имеют два неспаренных электрона; в рамках классических представлений это следовало бы интерпретировать так, будто в подобных молекулах каждый атом сохраняет неиспользованной одну свою Валентность (химич.), хотя нет никаких видимых препятствий для их использования.
До сих пор не решена проблема Валентность (химич.) в случае интерметаллических соединений (см. Металлиды, Металлическая связь), имеющих обычно сложный состав типа Cu5Zn8, Cu31Sn8, Zn21Fe5, нестехиометрических окислов, нитридов, карбидов, силицидов и других соединений металлов, в которых состав может меняться непрерывно в сравнительно широких пределах.
Таким образом, поиск общего определения Валентность (химич.), охватывающего все известные типы соединений и тем более способного предсказать возможность или принципиальную невозможность существования ещё не известных классов соединений, представляет сложную проблему. Конечно, параллельно с «неклассическими» соединениями химиками были синтезированы многие сотни тысяч соединений, которые могут быть интерпретированы в рамках обычных классических представлений о Валентность (химич.) Однако ясно, что все существующие частные определения Валентность (химич.) (см. раздел 1) ограничены определёнными классами и типами соединений, в которых преобладает какой-либо один тип химического взаимодействия. В общем же случае связи имеют промежуточный характер между чисто ионными и чисто ковалентными, в них принимают участие все типы взаимодействия одновременно, но в различных количественных соотношениях, резко изменяющихся от класса к классу и более плавно — от соединения к соединению внутри одного класса. При отсутствии общего определения Валентность (химич.) трудность заключается в том, чтобы определить границы, где перестаёт быть справедливым одно частное определение Валентность (химич.) и его заменяет другое. Решить эту проблему только на основании экспериментальных фактов и классических представлений невозможно. Существенную помощь здесь может оказать квантовая теория химической связи и Валентность (химич.)
Валентность (от лат. valentia — сила), способность атома к образованию химических связей. Количественной мерой В. обычно принято считать число других атомов в молекуле, с которыми данный атом образует связи. В. — одно из фундаментальных понятий теории химического строения (см. Химического строения теория). Оно формировалось вместе с понятием химической связи, параллельно с развитием синтетической химии и методов исследования строения и свойств веществ, и его содержание неоднократно расширялось и изменялось по мере того, как экспериментальная химия находила всё новые и новые классы соединений с неизвестными ранее типами взаимодействия атомов в молекуле, а в последние 30—40 лет — с развитием квантовой химии. В настоящее время накопленный химией экспериментальный материал столь обширен и разнообразен, а картина химической связи в разных соединениях столь пестра, что задача нахождения последовательного, единого и всеобъемлющего определения В. представляется крайне сложной. Эти трудности побуждают некоторых химиков вообще отказаться от поисков универсального понятия В. и заменить его набором более узких, но зато более конкретных и более точных понятий (ковалентность, гетеровалентность, координационное число и т.д.), область применимости каждого из которых ограничена соединениями с каким-либо одним преобладающим типом взаимодействия (ковалентным, ионным, координационным и т.д.). Однако до настоящего времени и в специальной, и в учебной литературе В. продолжает широко использоваться и как определение способности атома к образованию связей в самом общем смысле слова, и как количественная мера этой способности, и как синоним предлагаемых более узких понятий.
Единое и последовательное определение В. следует искать в рамках квантовохимической теории молекулярных орбиталей (см. Квантовая химия, Молекулярных орбиталей метод, Химическая связь, Молекула).
Для отдельных классов соединений, где преобладает какой-либо один тип химического взаимодействия, полезную информацию о способности атомов к образованию связей могут дать перечисленные ниже частные понятия (частные определения В.).
1. Определение понятия «валентность» и связь его с другими понятиями химии2. Эволюция понятия «валентность» и его роль в истории химии
3. Современные квантово-химические представления о валентности
|
Так же Вы можете узнать о... Квандо, Куанду (Kwando, Cuando), в нижнем течении — Линьянти, река в Анголе (в среднем течении пограничная между Анголой и Замбией), Намибии и Ботсване, правый приток Замбези. Ртутная турбина ,турбина, в которой рабочим телом является ртутный пар. Бакэу (уезд в Румынии) Бакэу (Bacau), уезд на В. Румынии. Площадь 6914 км2. Кудугу (Koudougou), город в Верхней Вольте, административный центр департамента Центральнозападный. Сорокин Питирим Александрович Сорокин (Sorokin) Питирим Александрович (21. Варшавское восстание 1944, антифашистское вооружённое выступление в Варшаве 1 августа — 2 октября 1944. Маркелиус Свен Маркелиус (Markelius) Свен (родился 25.10.1889, Стокгольм), шведский архитектор. Торндайк Сибил Торндайк (Thorndike) Сибил (р. 24.10.1882, Гейнсборо, графство Линкольншир), английская актриса. Гигрофиты (от гигро... и греч. phyton — растение), растения влажных местообитаний. Национальный музей (в Неаполе) Национальный музей (Museo Nazionale) в Неаполе, один из крупнейших музеев античного искусства в Италии. Хамаса, название антологий произведений арабской поэзии 6—9 вв. Добрынин Владимир Алексеевич [15(27).5.1895, Москва, — 20. Пастбищный хребет, горный хребет Большого Кавказа (в западной и центральной частях), протягивающийся севернее Скалистого хребта и имеющий характер куэсты. Щукин Степан Семенович [1758, Петербург, — 10(22). Иридоциты (от греч. iris, родительный падеж iridos — радуга и kуtos — вместилище, здесь — клетка), пигментные клетки, содержащие кристаллы гуанина, придающего блеск коже у рыб, земноводных и пресмыкающихся. |
|
 — атом Mo,
— атом Mo,  — атом Cl). Валентность (химич.)." alt="Рис. 2. Кластерная структура Mo6Cl4+8 (
— атом Cl). Валентность (химич.)." alt="Рис. 2. Кластерная структура Mo6Cl4+8 (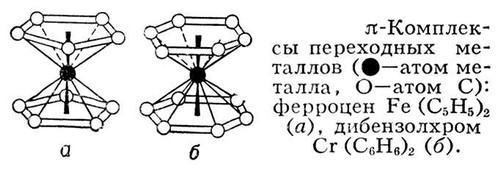 — атом металла,
— атом металла,  — атом С): ферроцен Fe(C5H5)2 (а), дибензолхром Cr(C6H6)2 (б). Валентность (химич.)." alt="Рис. 3. (
— атом С): ферроцен Fe(C5H5)2 (а), дибензолхром Cr(C6H6)2 (б). Валентность (химич.)." alt="Рис. 3. (