Ионный обмен
Большая Советская Энциклопедия. Статьи для написания рефератов, курсовых работ, научные статьи, биографии, очерки, аннотации, описания.
|
|
| ИОА |
| ИОВ |
| ИОГ |
| ИОД |
| ИОЗ |
| ИОК |
| ИОЛ |
| ИОМ |
| ИОН |
| ИОР |
| ИОС |
| ИОТ |
| ИОФ |
| ИОХ |
| ИОЦ |
Ионныйобмен, обмен ионов в растворах электролитов (гомогенный Ионный обмен о.). При смешении разбавленных растворов электролитов, например NaCl и KNO3 в смеси присутствуют ионы Na+, К+, NO3— и Cl—. Равновесное состояние выразится в этом случае уравнением: 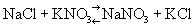 (реакция двойного обмена). Если одно из веществ, могущих получиться при взаимодействии, диссоциировано меньше других, равновесие сдвигается в сторону образования малодиссоциированного вещества. Равновесие сдвигается также в сторону образования летучего или малорастворимого продукта (если он выделяется из данной фазы) по реакциям:
(реакция двойного обмена). Если одно из веществ, могущих получиться при взаимодействии, диссоциировано меньше других, равновесие сдвигается в сторону образования малодиссоциированного вещества. Равновесие сдвигается также в сторону образования летучего или малорастворимого продукта (если он выделяется из данной фазы) по реакциям: 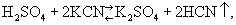
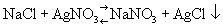
При выпаривании равновесного раствора прежде всего начинается кристаллизация соли (комбинации ионов), обладающей меньшей растворимостью. Избирательность кристаллизации может быть вызвана также добавлением органических растворителей (спирт, ацетон, диоксан и т. п.).
При гетерогенном Ионный обмен о. (ионообменная сорбция) обмен происходит между ионами, находящимися в растворе, и ионами, присутствующими на поверхности твёрдой фазы — ионита. При соприкосновении ионита, насыщенного одним ионом, например Н+, с раствором, содержащим другие ионы, например Na+ и Ca2+, происходит обмен ионов между раствором и ионитом: в растворе уменьшаются концентрации Na+ и Ca2+ и появляется эквивалентное количество ионов Н+.
Гетерогенный Ионный обмен о. имеет место при сорбции из растворов электролитов на некоторых минералах (алюмосиликатах, гидратах окисей металлов, цеолитах), в клетках и мембранах живых организмов и в синтетических ионообменных сорбентах. Гетерогенный Ионный обмен о. широко применяется для обессоливания воды, идущей для питания котлов паром высоких параметров, в гидрометаллургии, в химической и фармацевтической промышленности (см. Иониты).
|
Так же Вы можете узнать о... Маламуд Бернард Маламуд (Malamud) Бернард (родился 26.4.1914, Бруклин), американский писатель, Родился в еврейской семье иммигрантов. Матевосян Грант Игнатьевич (родился 3.3.1935, село Ахнидзор, ныне Туманянского района), армянский советский писатель. Мерида (город в Венесуэле) Мерида (Merida), город на З. Венесуэлы, административный центр штата Мерида. Мирный (город в Якутской АССР) Мирный, город республиканского (АССР) подчинения в Якутской АССР. Мормоны (Mormons; самоназвание «Latter Day Saints» — «Святые последнего дня»), члены религиозной секты, возникшей в США в 1-й половине 19 в. Мюнстер (Munster), город в ФРГ, в земле Северного Рейн-Вестфалия, на несудоходной р. Негус, негус негусов, титул императоров Эфиопии. «Новая жизнь» (большевистская газета) «Новая жизнь», первая легальная большевистская газета; выходила с 27 октября (9 ноября) по 3(16) декабря 1905 в Петербурге. Общенародное право, см. в ст. Право. Опробование месторождений полезных ископаемых, отбор и исследование проб из разных пунктов тел полезных ископаемых с целью определения их состава и качества. Охос-дель-Саладо (Ojos del Salado), потухший вулкан на Ю. Парфянский язык, язык парфян в период от начала 1-го тыс. Песталоцци Иоганн Генрих Песталоцци (Pestalozzi) Иоганн Генрих (12.1. Плеханово, посёлок городского типа в Ленинском районе Тульской области РСФСР. |
|