Кетоны
Большая Советская Энциклопедия. Статьи для написания рефератов, курсовых работ, научные статьи, биографии, очерки, аннотации, описания.
|
|
| КЕБ |
| КЕВ |
| КЕГ |
| КЕД |
| КЕЕ |
| КЕЗ |
| КЕЙ |
| КЕК |
| КЕЛ |
| КЕМ |
| КЕН |
| КЕП |
| КЕР |
| КЕС |
| КЕТ |
| КЕУ |
| КЕФ |
| КЕХ |
| КЕЦ |
| КЕЧ |
| КЕШ |
| КЕЭ |
Кетоны, класс органических соединений, содержащих карбонильную группу 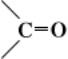 , связанную с двумя органическими радикалами, RCORў. В зависимости от природы R и R’ различают Кетоны алифатического (жирного), алициклического, ароматического или гетероциклического ряда. Так, простейший Кетоны жирного ряда — ацетон (диметилкетон) СН3СОСН3, ароматического ряда — бензофенон С6Н5СОС6Н5. В отличие от приведённых симметричных, существуют и несимметричные (смешанные) Кетоны, содержащие разные радикалы R и R’, например жирноароматические Кетоны — ацетофенон С6Н5СОСН3. Известны также многочисленные циклические Кетоны, у которых группа CO входит в цикл, например циклогексанон
, связанную с двумя органическими радикалами, RCORў. В зависимости от природы R и R’ различают Кетоны алифатического (жирного), алициклического, ароматического или гетероциклического ряда. Так, простейший Кетоны жирного ряда — ацетон (диметилкетон) СН3СОСН3, ароматического ряда — бензофенон С6Н5СОС6Н5. В отличие от приведённых симметричных, существуют и несимметричные (смешанные) Кетоны, содержащие разные радикалы R и R’, например жирноароматические Кетоны — ацетофенон С6Н5СОСН3. Известны также многочисленные циклические Кетоны, у которых группа CO входит в цикл, например циклогексанон 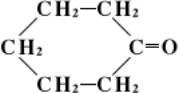
Наименования Кетоны жирного ряда по Женевской номенклатуре производят от названия соответствующих углеводородов, прибавляя окончание «он» и указывая место карбонильной группы; так, диэтилкетон CH3CH2COCH2CH3 называют пентанон-3.
Низшие алифатические Кетоны — бесцветные жидкости с приятным запахом, смешивающиеся с водой; высшие — твёрдые вещества. Все Кетоны растворимы в органических растворителях.
По способам получения и свойствам Кетоны аналогичны альдегидам; однако Кетоны менее реакционноспособны, значительно более устойчивы к окислению. Для Кетоны характерны два вида реакций, обусловленных наличием карбонильной группы, — присоединение к карбонильной группе и замещение её атома кислорода. Так, к Кетоны легко присоединяется синильная кислота HCN с образованием оксинитрилов RC (OH) RўCN; аналогично с Кетоны реагируют бисульфит натрия NaHSO3, хлороформ CHCl3 и др. При гидрировании Кетоны образуются вторичные спирты: RCORў+H2® RCH (OH) Rў,
при взаимодействии Кетоны с металлоорганическими соединениями и последующем гидролизе — третичные спирты: RCOR’+R’’MgX ® RR’C(R’’)OmgX ® RR’R’’COH.
При взаимодействии с PCI5 атом кислорода в Кетоны замещается на два атома хлора. С гидроксиламином Кетоны дают кетоксимы: RCOR’+NH2OH ® RC (=NOH) R’;
эту реакцию, а также образование др. кристаллических продуктов замещения кислорода (например, гидразонов, 2,4-динитро-фенилгидразонов) применяют для идентификации Кетоны Гидролиз этих продуктов используется для получения чистых Кетоны Большое значение имеет восстановление группы 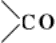 до
до 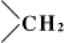 (Кижнера —Вольфа реакция).
(Кижнера —Вольфа реакция).
В промышленности Кетоны получают дегидрированием вторичных спиртов: RCH (OH) R’ ® RCOR’+H2
термическим разложением кальциевых солей карбоновых кислот: (RCOO)2Ca ® R2CO+CaCO3
или пропусканием паров карбоновых кислот над катализаторами типа окисей тория, бария, а также карбоната кальция. Ароматические и жирноароматические Кетоны получают при действии на ароматические углеводороды хлорангидридов кислот в присутствии хлористого алюминия, например: C6H6+CH3COCl ® C6H5COCH3+HCl.
Многие Кетоны можно получать окислением углеводородов кислородом воздуха в присутствии катализаторов: например, из этилбензола C6H5CH2CH3 получают ацетофенон, из циклогексана — циклогексанон.
Кетоны находят разнообразное применение. Так, циклогексанон служит исходным продуктом для получения синтетических волокна капрона. Михлера кетон применяют в производстве триарилметановых красителей. Некоторые Кетоны используют в парфюмерии (см. Иононы).
Лит.: Несмеянов А. Н., Несмеянов Н. А., Начала органической химии, кн. 1—2, М., 1969—70.
|
Так же Вы можете узнать о... Драный Семен Алексеевич Драный Семён Алексеевич (1667—1708), один из предводителей Булавинского восстания 1707—09. Жекитиньонья (Jequitinhonha), река на В. Бразилии. Звенигород Киевский древнерусский город-крепость, прикрывавший Киев с юго-востока. Ижморский, посёлок городского типа, центр Ижморского района Кемеровской области РСФСР. Ионный источник, устройство для получения направленных потоков (пучков) ионов. Калийные соли, калиевые соли, осадочные хемогенные горные породы, образованные легко растворимыми в воде калиевыми и калиево-магниевыми минералами. Карльскуга (Karlskoga), город в центральной Швеции, в лене Эребру, у озера Мёккельн. Кешью, кажу, анакард, акажу (Anacardium occidentale), дерево высотой до 12 м из семейства сумаховых. Ковтюх Епифан Иович [9(21).5.1890 — 28.7.1938], советский военачальник, комкор (1935). Конкордат (позднелатинское concordatum — соглашение, от латинского concordo — нахожусь в согласии), соглашение между папой римским как главой католической церкви и католическим государством, регулирующее положение католической церкви в этом государстве, её права в области брачно-семейных отношений, в школьном вопросе и т. Котлетный автомат, машина, дозирующая и формующая котлеты из фарша. Крючковидные отростки, выросты грудных рёбер, костные — у птиц и некоторых ископаемых пресмыкающихся, хрящевые — у современных пресмыкающихся (крокодилы, гаттерия). Лазарев (антарктич. научн. станция) Лазарев, антарктическая научная станция СССР, действовавшая с 10 марта 1959 по 26 февраля 1961 на шельфовом леднике Лазарева (Берег Принцессы Астрид, Восточная Антарктида) на 69°58' южной широты и 12°55' восточной долготы. Лесопропускные сооружения, гидротехнические сооружения для пропуска сплавляемого леса (в плотах или россыпью) через плотины и др. Лоран Огюст Лоран (Laurent) Огюст (14.11.1807, Ла-Фоли, — 15. Макк фон Лайберих Карл Макк фон Лайберих (Mack von Leiberich) Карл (24. |
|