Сигма- и пи-связи
Большая Советская Энциклопедия. Статьи для написания рефератов, курсовых работ, научные статьи, биографии, очерки, аннотации, описания.
|
|
| СИА |
| СИБ |
| СИВ |
| СИГ |
| СИД |
| СИЕ |
| СИЗ |
| СИИ |
| СИЙ |
| СИК |
| СИЛ |
| СИМ |
| СИН |
| СИО |
| СИП |
| СИР |
| СИС |
| СИТ |
| СИУ |
| СИФ |
| СИХ |
| СИЦ |
| СИШ |
| СИЭ |
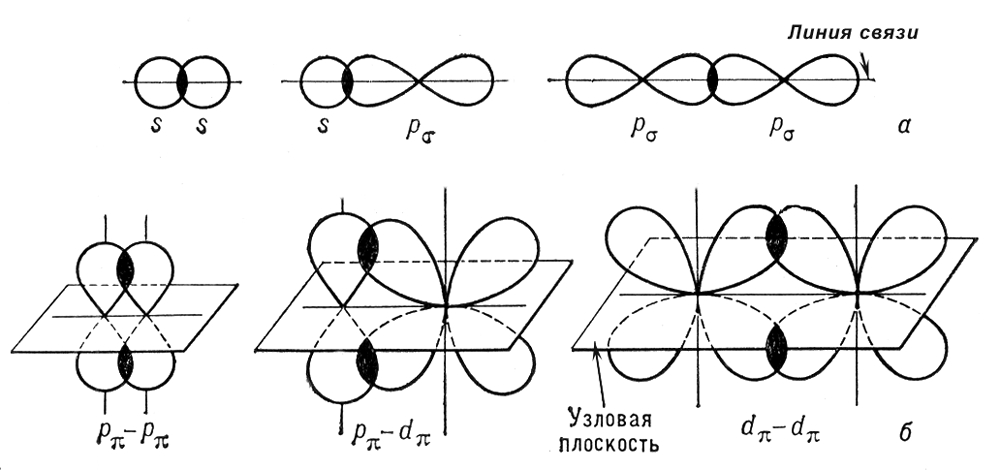
Сигмаи пи-связи (sи p-связи), ковалентные химические связи, характеризующиеся определенней, но различной пространственной симметрией распределения электронной плотности. Как известно, ковалентная связь образуется в результате обобществления электронов взаимодействующих атомов. Результирующее электронное облако s-связи симметрично относительно линии связи, т. е. линии, соединяющей ядра взаимодействующих атомов. Простые связи в химических соединениях обычно являются (т-связями (см. Простая связь). Электронное облако p-связи симметрично относительно плоскости, проходящей через линию связи (рис. 1, б), причём в этой плоскости (называемой узловой) электронная плотность равна нулю. Употребление греческих букв s и p связано с соответствием их латинским буквам s и р в обозначении электронов атома, при участии которых впервые появляется возможность для образования sи p-связей соответственно. Поскольку облака атомных р-орбиталей (px, ру, pz) симметричны относительно соответствующих осей декартовых координат (х, у, z), то, если одна р-орбиталь, например pz, принимает участие в образовании s-связи (ось z — линия связи), две оставшиеся р-орбитали (px, py) могут принять участие в образовании двух p-связей (их узловые плоскости будут yz и xz соответственно; см. рис. 2). В образовании s и p-связей могут принять участие также d(см. рис. 1) и f-электроны атома.
Рис. 1. Схематическое изображение пространственной ориентации орбиталей при образовании s-связи в результате s — s-, s — ps-, ps — ps-взаимодействий (а) и p-связи в результате pp — , pp — , dp — dp — взаимодействий (б).
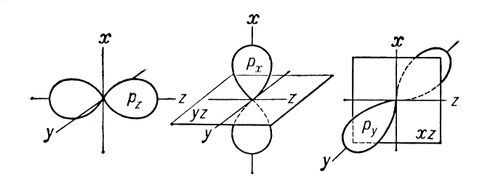
Рис. 2. Схематическое изображение облаков px-, ру-, pzэлектронов. Показаны оси декартовых координат и узловые плоскости pxи ру-орбиталей.
Если между атомами в молекуле возникают одновременно как s-, так и p-связи, то результирующая связь является кратной (см. Кратные связи, Двойная связь, Тройная связь, а также Валентность).
Лит.: Пиментел Г., Спратли Р., Как квантовая механика объясняет химическую связь, пер. с англ., М., 1973; Шусторович Е. М., Химическая связь, М., 1973.
Е. М. Шусторович.
|
Так же Вы можете узнать о... Рихтер Ханс Вернер Рихтер (Richter) Ханс Вернер (р. 12.11.1908, Банзин, остров Узедом), немецкий писатель (ФРГ). Совпадений схема, электронное устройство, служащее для выделения из совокупности поступающих на него сигналов (электрических импульсов) только таких, которые полностью либо частично перекрываются (совпадают) во времени; представляет собой коммутирующее устройство дискретного действия с несколькими входами и одним выходом, сигнал на котором появляется только тогда, когда есть сигналы на всех входах одновременно. Токтогульская ГЭС, гидроэлектростанция на р. Хабаров Ерофей Павлович Хабаров (по прозвищу Святитский) Ерофей Павлович (около 1610, деревня Дмитриево, ныне Нюксенского района Вологодской области, — после 1667), русский крестьянин мореход и землепроходец. Щербина Фёдор Андреевич [1(13).2.1849, станица Новодеревянковская на Кубани,— 1936, Прага], земский статистик, народник, член-корреспондент Петербургской АН (1904). Амур-Санан Антон Мудренович [14 (26).9.1888, Багабуруловский аймак, ныне Городовиковского района Калмыкской АССР, — 17. Богородицкий Василий Алексеевич [7(19).4.1857, Царевококшайск, ныне Йошкар-Ола, — 23. Вскрытие рек, процесс разрушения ледяного покрова, происходящий под воздействием тепла и механических сил, возникающих в результате интенсивного притока воды. Дваравати, древнее монское (см. Моны) государство в Юго-Восточной Азии, существовавшее до 10 в. Зоологические музеи, научные и культурно-просветительские учреждения, в которых сосредоточены коллекции животных (в фиксирующих жидкостях, высушенные или особо препарированные животные, их чучела, скелеты, шкуры, а также изделия из рога, кости, раковин и т. «Киргизфильм», киностудия в Киргизской ССР. Находится в г. Лактатдегидрогеназа, фермент класса оксидоредуктаз; катализирует обратимое восстановление пировиноградной кислоты до L-молочной кислоты с потреблением в качестве кофермента восстановленного никотинамидадениндинуклеотида (НАД×Н+Н+): Нотариат (от лат. notarius — писец, секретарь), система органов, в функции которых входит удостоверение сделок, оформление наследств. |
|