Энтальпия
Большая Советская Энциклопедия. Статьи для написания рефератов, курсовых работ, научные статьи, биографии, очерки, аннотации, описания.
|
|
| ЭНА |
| ЭНВ |
| ЭНГ |
| ЭНД |
| ЭНЕ |
| ЭНЗ |
| ЭНИ |
| ЭНК |
| ЭНЛ |
| ЭНН |
| ЭНО |
| ЭНР |
| ЭНС |
| ЭНТ |
| ЭНУ |
| ЭНФ |
| ЭНЦ |
Энтальпия (от греч. enthálpo — нагреваю) (теплосодержание, тепловая функция Гиббса), потенциал термодинамический, характеризующий состояние термодинамической системы при выборе в качестве основных независимых переменных энтропии S и давления р. Обозначается H (S, р, N, xl), где N — число частиц системы, xi — другие макроскопические параметры системы. Энтальпия — аддитивная функция, т. е. Энтальпия всей системы равна сумме Энтальпия составляющих её частей; с внутренней энергией U системы Энтальпия связана соотношением H = U + pV, (1)
где V — объём системы. Полный дифференциал Энтальпия (при неизменных N и xi) имеет вид:
dH = TdS + Vdp. (2)
Из формулы (2) можно определить температуруТ и объем системы: 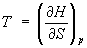 ,
, 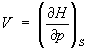 .
.
При постоянном давлении (р = const.) теплоемкость системы 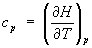
Эти свойства Энтальпия при р = const аналогичны свойствам при постоянном объеме: 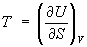 ,
, 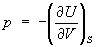 и
и 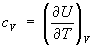 .
.
Равновесному состоянию системы в условиях постоянства S и р соответствует минимальное значение Энтальпия Изменение Энтальпия (DН) равно количеству теплоты, которое сообщают системе или отводят от нее при постоянном давлении, поэтому значения DН характеризуют тепловые эффекты фазовых переходов (плавления, кипения и т. д.), химических реакций и других процессов, протекающих при постоянном давлении. При тепловой изоляции тел (в условиях р = const) Энтальпия сохраняется, поэтому ее называют иногда теплосодержанием или тепловой функцией. Условие сохранения Энтальпия лежит, в частности, в основе теории Джоуля — Томсона эффекта, нашедшего важное практическое применение при сжижении газов. Термин «Энтальпия» был предложен Х. Камерлинг-Оннесом.
Д. Н. Зубарев.
|
Так же Вы можете узнать о... Природопользование, совокупность воздействий человечества на географическую оболочку Земли, рассматриваемая в комплексе (в отличие от отраслевых понятий — водопользование, землепользование, лесопользование и др. Социология (франц. sociologie, от лат. socictas — общество и греч. Фосфаты калия, калиевые соли фосфорных кислот, см. Авиационная промышленность, зародилась в начале 20 в. Бутирометр (от греч. Butyron — масло и ...метр), жиромер, прибор для измерений жирности молока. Двин, Востан, крупный ремесленно-торговый город, центр транзитной торговли Армении в 4—13 вв. Карельский перешеек, перешеек между Финским заливом Балтийского моря и Ладожским озером, в Ленинградской обл. Лонг-Айленд (Long Island), остров в Атлантическом океане, у берегов США, близ устья реки Гудзон. «Обсервер» («The Observer» — «Наблюдатель»), английская воскресная газета. Рамадан, рамазан, девятый месяц мусульманского лунного календаря; см. Сулак (пос. гор. типа в Дагестанской АССР) Сулак, посёлок городского типа в Дагестанской АССР, подчинён Советскому райсовету г. Хомутовка, посёлок городского типа, центр Хомутовского района Курской области РСФСР. Американо-мексиканская война 1846-48 Американо-мексиканская война 1846—48, захватническая война США против Мексики. |
|