Диаграмма состояния
Большая Советская Энциклопедия. Статьи для написания рефератов, курсовых работ, научные статьи, биографии, очерки, аннотации, описания.
|
|
| ДИА |
| ДИБ |
| ДИВ |
| ДИГ |
| ДИД |
| ДИЕ |
| ДИЖ |
| ДИЗ |
| ДИИ |
| ДИК |
| ДИЛ |
| ДИМ |
| ДИН |
| ДИО |
| ДИП |
| ДИР |
| ДИС |
| ДИТ |
| ДИУ |
| ДИФ |
| ДИХ |
| ДИЦ |
| ДИЧ |
| ДИЭ |
| ДИЯ |
Диаграмма состояния, диаграмма равновесия, фазовая диаграмма, графическое изображение соотношений между параметрами состояния физико-химической системы (температурой, давлением и др.) и её составом. В простейшем случае, когда система состоит только из одного компонента, Диаграмма состояния представляет собой трёхмерную пространственную фигуру, построенную в трёх прямоугольных координатных осях, по которым откладывают температуру (Т), давление (p) и мольный объём (v). Пользование объёмной Диаграмма состояния неудобно вследствие её громоздкости; поэтому на практике применяют проекцию Диаграмма состояния на одну из координатных плоскостей, обычно на плоскость p — Т.
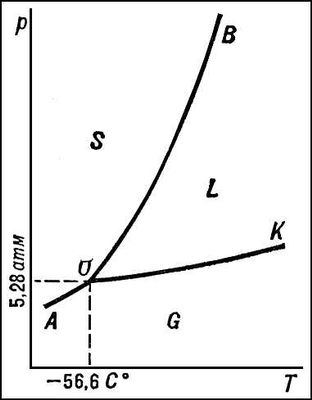
Диаграмма состояния двуокиси углерода CO2.
В качестве простейшего примера на рис. изображена (без соблюдения масштаба) Диаграмма состояния двуокиси углерода CO2. Любая точка Диаграмма состояния (фигуративная точка) изображает состояние CO2 при температуре и давлении, отвечающих этой точке. Точка О (тройная точка) отвечает равновесию трёх фаз — твёрдой, жидкой и газообразной CO2. В точке О пересекаются три кривые: ОА (кривая возгонки), отвечающая равновесиям твёрдой и газообразной CO2; OK (кривая испарения), отвечающая равновесиям жидкой и газообразной CO2; ОВ (кривая плавления) — твёрдой и жидкой CO2. Эти кривые делят плоскость диаграммы на три поля — области существования трёх фаз: твёрдой S, жидкой L и газообразной G. Точка К отвечает критической температуре CO2 (31,0°С), при которой исчезает различие между свойствами жидкости и газа. Согласно терминологии фаз правила, точке О отвечает нонвариантное равновесие, точкам на кривых ОА, ОВ и ОК — моновариантное равновесие, а точкам на полях S, L и G — дивариантное равновесие. В случае полиморфизма Диаграмма состояния усложняется (число тройных точек равно числу полиморфных превращений). О Диаграмма состояния систем, число компонентов которых больше 1, см. в статье Двойные системы.
Экспериментальное построение Диаграмма состояния осуществляется различными методами физико-химического анализа, термических и рентгенографических анализов, оптической и электронной микроскопии, дилатометрии, измерения электросопротивления, твёрдости и др. свойств. Правильность построения Диаграмма состояния проверяется на основании правила фаз, принципа соответствия и принципа непрерывности. Диаграмма состояния широко применяют на практике в металловедении, металлургии, химии и др.; например, Диаграмма состояния железо — углерод имеет важное значение для термической обработки стали.
Лит.: Аносов В. Я., Погодин С. А., Основные начала физико-химического анализа, М.—Л., 1947; Аносов В. Я., Краткое введение в физико-химический анализ, М., 1959; Древинг В. П., Калашников Я. А., Правило фаз с изложением основ термодинамики, 2 изд., М., 1964.
С. А. Погодин.
|
Так же Вы можете узнать о... Ватер Александр де Ватер (Vathaire) Александр де (гг. рождения и смерти неизвестен), французский металлург. Дербник (Falco columbarius), птица семейства соколиных отряда хищных. Касансай (пос. гор. типа в Узбекской ССР) Касансай, посёлок городского типа в Чустском районе Наманганской области Узбекской ССР. Лорантовые, семейство двудольных растений; то же, что ремнецветниковые. О-хлорбензальмалонодинитрил, см. Орто-хлорбензальмалонодинитрил. Рабочее время, 1) мера продолжительности участия работника в общественно организованном труде; установленное законом или на основе закона время, в течение которого работник должен выполнять свои трудовые обязанности. Стереомодель, объёмный (рельефный) образ объекта или участка местности, возникающий у наблюдателя при рассматривании двух плоских перспективных изображений, полученных с различных точек пространства. Хайфон (Hai Phong), город во Вьетнаме, в дельте р. Аджарисцкали, Ачарисцкали, река в Аджарской АССР, правый приток р. Бюджетная система, совокупность бюджетов государства, административно-территориальных единиц и бюджетов (смет) и счетов автономных в бюджетном отношении учреждений и фондов, основанная на экономических отношениях и юридических нормах. Дафни (Daphni), монастырь в Греции, в 10 км от Афин. Капитализм, общественно-экономическая формация, основанная на частной собственности на средства производства и эксплуатации наёмного труда капиталом; сменяет феодализм, предшествует социализму — первой фазе коммунизма. Лингнер Макс Лингнер (Lingner) Макс (17.11.1888, Лейпциг, — 14. Новая Маячка, посёлок городского типа в Цюрупинском районе Херсонской области УССР, в 29 км от ж. |
|