Биоэлектрические потенциалы
Большая Советская Энциклопедия. Статьи для написания рефератов, курсовых работ, научные статьи, биографии, очерки, аннотации, описания.
|
|
| БИА |
| БИБ |
| БИВ |
| БИГ |
| БИД |
| БИЕ |
| БИЖ |
| БИЗ |
| БИИ |
| БИЙ |
| БИК |
| БИЛ |
| БИМ |
| БИН |
| БИО |
| БИП |
| БИР |
| БИС |
| БИТ |
| БИУ |
| БИФ |
| БИХ |
| БИЦ |
| БИЧ |
| БИШ |
| БИЭ |
| БИЮ |
| БИЯ |
Биоэлектрические потенциалы, электрические потенциалы, возникающие в тканях и отдельных клетках человека, животных и растений, важнейшие компоненты процессов возбуждения и торможения. Исследование Биоэлектрические потенциалы имеет большое значение для понимания физико-химических и физиологических процессов в живых системах и применяется в клинике с диагностической целью (электрокардиография,электроэнцефалография,электромиография и др.).
Первые данные о существовании Биоэлектрические потенциалы («животного электричества») были получены в 3-й четверти 18 в. при изучении природы «удара», наносимого некоторыми рыбами с электрическими органами при защите или нападении. К этому же времени относится начало исследований итальянского физиолога и врача Л. Гальвани, заложивших основу учения о Биоэлектрические потенциалы Многолетний научный спор (1791—97) между Л. Гальвани и физиком А. Вольта о природе «животного электричества» завершился двумя крупными открытиями: были получены факты о существовании биоэлектрических явлений в живых тканях и открыт новый принцип получения электрического тока с помощью разнородных металлов — создан гальванический элемент (вольтов столб). Правильная оценка наблюдений Гальвани стала возможной лишь после применения достаточно чувствительных электроизмерительных приборов — гальванометров. Первые такие исследования были проведены итальянским физиком К. Маттеуччи (1837). Систематическое изучение Биоэлектрические потенциалы было начато немецким физиологом Э. Дюбуа-Реймоном (1848), который доказал существование Биоэлектрические потенциалы в нервах и мышцах в покое и при возбуждении. Но ему не удалось (в силу большой инерционности гальванометра) зарегистрировать быстрые, длящиеся тысячные доли сек колебания Биоэлектрические потенциалы при проведении импульсов вдоль нервов и мышц. В 1886 немецкий физиолог Ю. Бернштейн проанализировал форму потенциала действия; французский учёный Э. Ж. Марей (1875) применил для записи колебаний потенциалов бьющегося сердца капиллярный электрометр; русский физиолог Н. Е. Введенский использовал (1883) для прослушивания ритмических разрядов импульсов в нерве и мышце телефон, а голландский физиолог В. Эйнтховен (1903) ввёл в эксперимент и клиническую практику струнный гальванометр — высокочувствительный и малоинерционный прибор для регистрации электрических токов в тканях. Значительный вклад в изучение Биоэлектрические потенциалы внесли русские физиологи: В. В. Правдич-Неминский (1913—21) впервые зарегистрировал электроэнцефалограмму, А. Ф. Самойлов (1929) исследовал природу нервно-мышечной передачи возбуждения, а Д. С. Воронцов (1932) открыл следовые колебания Биоэлектрические потенциалы, сопровождающие потенциал действия в нервных волокнах. Дальнейший прогресс в изучении Биоэлектрические потенциалы был тесно связан с успехами электроники, позволившими применить в физиологическом эксперименте электронные усилители и осциллографы (работы американских физиологов Г. Бишопа, Дж. Эрлангера и Г. Гассера в 30—40-х гг. 20в.). Изучение Б.п. в отдельных клетках и волокнах стало возможным с разработкой микроэлектродной техники. Важное значение для выяснения механизмов генерации Биоэлектрические потенциалы имело использование гигантских нервных волокон головоногих моллюсков, главным образом кальмара. Диаметр этих волокон в 50 — 100 раз больше, чем у позвоночных животных, он достигает 0,5—1 мм, что позволяет вводить внутрь волокна микроэлектроды, инъецировать в протоплазму различные вещества и т.п. Изучение ионной проницаемости мембраны гигантских нервных волокон позволило английским физиологам А. Ходжкину, А. Хаксли и Б. Катцу (1947—52) сформулировать современную мембранную теорию возбуждения.
Различают следующие основные виды Б. п. нервных и мышечных клеток: потенциал покоя, потенциал действия, возбуждающие и тормозные постсинаптические потенциалы, генераторные потенциалы.
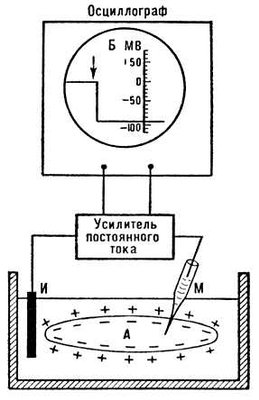
Потенциал покоя (ПП, мембранный потенциал покоя). У живых клеток в покое между внутренним содержимым клетки и наружным раствором существует разность потенциалов (ПП) порядка 60—90мв, которая локализована на поверхностной мембране. Внутренняя сторона мембраны заряжена электроотрицательно по отношению к наружной (рис. 1). ПП обусловлен избирательной проницаемостью покоящейся мембраны для ионов К+ (Ю. Бернштейн, 1902, 1912; А. Ходжкин и Б. Катц, 1947). Концентрация К+ в протоплазме примерно в 50 раз выше, чем во внеклеточной жидкости, поэтому, диффундируя из клетки, ионы выносят на наружную сторону мембраны положительные заряды, при этом внутренняя сторона мембраны, практически не проницаемой для крупных органических анионов, приобретает отрицательный потенциал. Поскольку проницаемость мембраны в покое для Na+ примерно в 100 раз ниже, чем для К+, диффузия натрия из внеклеточной жидкости (где он является основным катионом) в протоплазму мала и лишь незначительно снижает ПП, обусловленный ионами К+. В скелетных мышечных волокнах в возникновении потенциала покоя важную роль играют также ионы Cl-, диффундирующие внутрь клетки. Следствием ПП является ток покоя, регистрируемый между поврежденным и интактным участками нерва или мышцы при приложении отводящих электродов. Мембраны нервных и мышечных клеток (волокон) способны изменять ионную проницаемость в ответ на сдвиги мембранного потенциала. При увеличении ПП (гиперполяризация мембраны) проницаемость поверхностных клеточных мембран для Na+ и К+ падает, а при уменьшении ПП (деполяризация) она возрастает, причём скорость изменений проницаемости для Na+ значительно превышает скорость увеличения проницаемости мембраны для К+.
Рис. 1. Схема измерений мембранного потенциала покоя с помощью внутриклеточного стеклянного микроэлектрода (М). Второй электрод (И) помещен в омывающую клетку жидкость.
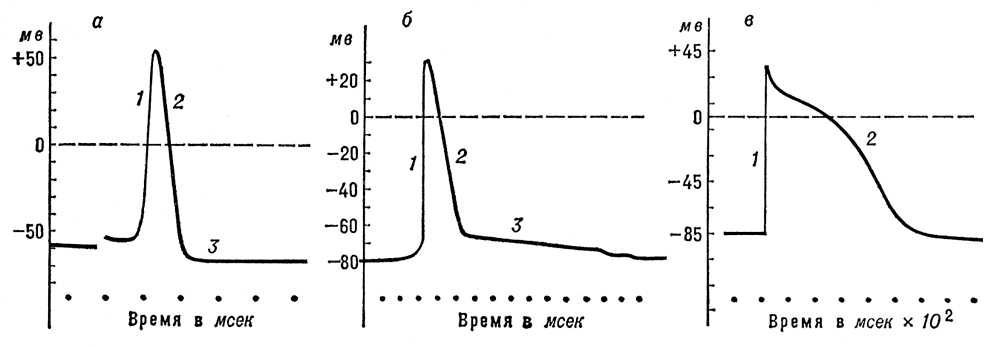
Потенциал действия (ПД). Все раздражители, действующие на клетку, вызывают в первую очередь снижение ПП; когда оно достигает критического значения (порога), возникает активный распространяющийся ответ — ПД (рис. 2). Во время восходящей фазы ПД кратковременно извращается потенциал на мембране: её внутренняя сторона, заряженная в покое электроотрицательно, приобретает в это время положительный потенциал. Достигнув вершины, ПД начинает падать (нисходящая фаза ПД), и потенциал на мембране возвращается к уровню, близкому к исходному, — ПП. Полное восстановление ПП происходит только после окончания следовых колебаний потенциала — следовой деполяризации или гиперполяризации, длительность которых обычно значительно превосходит продолжительность пика ПД. Согласно мембранной теории, деполяризация мембраны, вызванная действием раздражителя, приводит к усилению потока Na+ внутрь клетки, что уменьшает отрицательный потенциал внутренней стороны мембраны — усиливает её деполяризацию. Это, в свою очередь, вызывает дальнейшее повышение проницаемости для Na+ и новое усиление деполяризации и т.д. В результате такого взрывного кругового процесса, т. н. регенеративной деполяризации, происходит извращение мембранного потенциала, характерное для ПД. Повышение проницаемости для Na+ очень кратковременно и сменяется её падением (рис. 3), а следовательно, уменьшением потока Na+ внутрь клетки. Проницаемость для К+, в отличие от проницаемости для Na+, продолжает увеличиваться, что приводит к усилению потока К+ из клетки. В результате этих изменений ПД начинает падать, что ведёт к восстановлению ПП. Таков механизм генерации ПД в большинстве возбудимых тканей. Существуют, однако, клетки (мышечные волокна ракообразных, нервные клетки у ряда брюхоногих моллюсков, некоторые растительные клетки), у которых восходящая фаза ПД обусловлена повышением проницаемости мембраны не для ионов Na+, а для ионов Ca+. Своеобразен также механизм генерации ПД в мышечных волокнах сердца, для которых характерно длительное плато на нисходящей фазе ПД (рис. 2, б). Неравенство концентраций ионов К+ и Na+ (или Ca+) внутри и снаружи клетки (волокна) поддерживается специальным механизмом (т. н. «натриевым насосом»), выталкивающим ионы Na+ из клетки и нагнетающим ионы К+ в протоплазму, требующим затраты энергии, которая черпается клеткой в процессах обмена веществ.
Рис. 2. Потенциалы действия, зарегистрированные с помощью внутриклеточных микроэлектродов: а — гигантского аксона кальмара; б — скелетного мышечного волокна; в — волокна мышцы сердца собаки; 1 — восходящая фаза ПД; 2 — нисходящая фаза; 3 — следовая гиперполяризация (а) и следовая деполяризация (б).
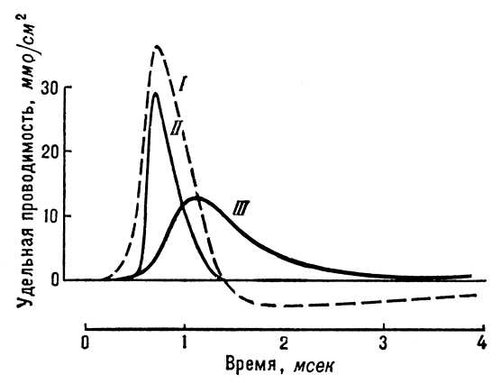
Рис. 3. Изменения натриевой и калиевой проводимости мембраны нервного волокна во время генерации потенциала действия (I). Изменения проводимости пропорциональны изменениям проницаемости для Na+(II) и К+(III).
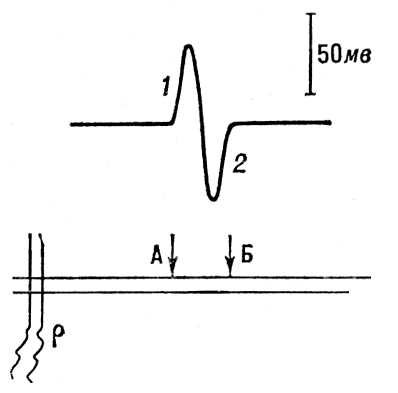
Амплитуда ПД большинства нервных и мышечных волокон примерно одинакова: 110—120 мв. Длительность ПД варьирует в широких пределах: у теплокровных животных длительность ПД нервных волокон, наиболее быстро проводящих возбуждение, — 0,3—0,4 мсек, у волокон же мышц сердца — 50—600 мсек. В растительных клетках пресноводной водоросли хара ПД продолжается около 20 сек. Характерной особенностью ПД, отличающей его от других форм ответа клетки на раздражение, является то, что он подчиняется правилу «всё или ничего», т. е. возникает только при достижении раздражителем некоторого порогового значения, и дальнейшее увеличение интенсивности раздражителя уже не сказывается ни на амплитуде, ни на продолжительности ПД. Потенциал действия — один из важнейших компонентов процесса возбуждения. В нервных волокнах он обеспечивает проведение возбуждения от чувствительных окончаний (рецепторов) к телу нервной клетки и от неё — к синаптическим окончаниям (см. Синапсы), расположенным на различных нервных, мышечных или железистых клетках. Поступая в эффекторные окончания, ПД вызывает выделение (секрецию) определённой порции специфических химических веществ, т. н. медиаторов, оказывающих возбуждающее или тормозящее влияние на соответствующие клетки. В мышечных волокнах распространяющийся ПД вызывает цепь физико-химических реакций, лежащих в основе процесса сокращения мышц. Проведение ПД вдоль нервных и мышечных волокон осуществляется т. н. локальными токами, или токами действия, возникающими между возбуждённым (деполяризованным) и соседними с ним покоящимися участками мембраны (см. Возбуждение). Токи действия регистрируются обычными внеклеточными электродами; при этом кривая имеет двухфазный характер: первая фаза соответствует приходу ПД под ближний электрод, вторая — под дальний электрод (рис. 4).
Рис. 4. Регистрация распространения потенциала действия вдоль нервного волокна. А, Б — внеклеточные электроды; р — раздражающие электроды. Вверху — отклонение луча осциллографа под влиянием волны возбуждения; 1 — волна возбуждения под электродом А; 2 — под электродом Б.
Постсинаптические потенциалы (ПСП) возникают в участках мембраны нервных или мышечных клеток, непосредственно граничащих с синаптическими окончаниями. Они имеют амплитуду порядка нескольких мв и длительность 10—15 мсек. ПСП подразделяются на возбуждающие (ВПСП) и тормозные (ТПСП). ВПСП представляют собой местную деполяризацию постсинаптической мембраны, обусловленную действием соответствующего медиатора (например, ацетилхолина в нервно-мышечном соединении). При достижении ВПСП некоторого порогового (критического) значения в клетке возникает распространяющийся ПД (рис. 5, а, б). ТПСП выражается местной гиперполяризацией мембраны, обусловленной действием тормозного медиатора (рис. 5, в). В отличие от ПД, амплитуда ПСП постепенно увеличивается с увеличением количества выделившегося из нервного окончания медиатора. ВПСП и ТПСП суммируются друг с другом при одновременном или последовательном поступлении нервных импульсов к окончаниям, расположенным на мембране одной и той же клетки.
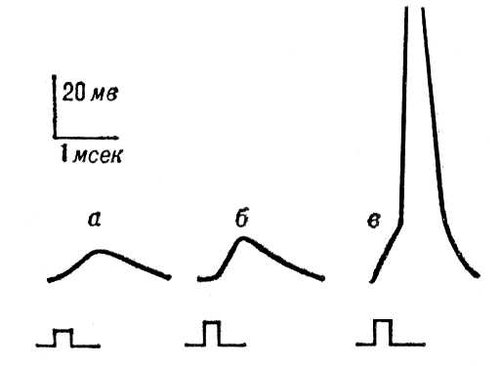
Рис. 5. Постсинаптические потенциалы: а — подпороговые ВПСП, возникающие в нервной клетке в ответ на раздражения соответствующих нервных волокон; б — ВПСП, достигший порогового значения, достаточного для возникновения ПД; в — ТПСП, вызванный раздражением тормозных нервных волокон.
Генераторные потенциалы возникают в мембране чувствительных нервных окончаний — рецепторов. Они внешне сходны с ВПСП — их амплитуда порядка нескольких мв и зависит от силы приложенного к рецептору раздражения (рис. 6). Когда генераторный потенциал достигает порогового (критического) значения, в соседнем участке мембраны нервного волокна возникает распространяющийся ПД. Ионный механизм генераторных потенциалов ещё недостаточно изучен.
Рис. 6. Генераторные потенциалы: увеличение амплитуды при усилении раздражения рецептора (а — в). При достижении порогового значения (в) генераторный потенциал вызвал в чувствительном нервном волокне потенциал действия.
Наряду с перечисленными относительно быстро развивающимися Биоэлектрические потенциалы, в нервных клетках, волокнах гладких мышц и некоторых растительных клетках регистрируются также очень медленные колебания мембранного потенциала неизвестной природы, причём на гребне волны деполяризации мембраны часто возникают разряды импульсов.
Все Биоэлектрические потенциалы могут быть зарегистрированы и точно измерены только с помощью внутриклеточных микроэлектродов, позволяющих отводить разности потенциалов между внутренней и наружной сторонами мембраны клетки. При отведении колебаний Биоэлектрические потенциалы от целых нервов, мышц или мозга с помощью поверхностных электродов регистрируется лишь суммарно потенциал множества синхронно или, чаще, асинхронно работающих клеток. Так, электромиограмма представляет собой результат сложения (интерференции) ПД множества скелетных мышечных волокон; электрокардиограмма — результирующая колебаний электрических потенциалов мышечных волокон различных отделов сердца; электроэнцефалограмма — результат суммации главным образом ВПСП и ТПСП множества клеток различных слоев коры больших полушарий. Регистрация таких интерференционных электрограмм, хотя и не позволяет анализировать колебания Биоэлектрические потенциалы отдельных клеток, имеет важное значение для суждения о состоянии исследуемого органа в целом. В клинической практике электромиограмму, электрокардиограмму и электроэнцефалограмму регистрируют с помощью электродов, расположенных на коже соответствующих частей тела. Оценка данных, полученных этими методами, основана на сопоставлении изменений характера соответствующей кривой с результатами клинических, физиологических и патологоанатомических исследований.
Лит.; Физиология человека, М., 1966; Гальвани Л. и Вольта А., Избр. работы о животном электричестве, М. — Л., 1937; Ходжкин А., Нервный импульс, пер. с англ., М., 1965; Экклс Дж., Физиология нервных клеток, пер. с англ., М., 1959; его же, Физиология синапсов, М., 1966; Катц Б., Нерв, мышца и синапс, пер. с англ., М., 1968; Ходоров Б. И., Проблема возбудимости, Л., 1969.
Б. И. Ходоров.
|
Так же Вы можете узнать о... Клостридии (Clostridium; от греч. kloster — веретено), род спороносных бактерий. Мимика (от греч. mimikos — подражательный), выразительные движения мышц лица, являющиеся одной из форм проявления тех или иных чувств, настроений человека. Полупроводники, широкий класс веществ, характеризующихся значениями электропроводности s, промежуточными между электропроводностью металлов (s ~ 106—104ом-1 см-1) и хороших диэлектриков (s£ 10-10—10-12ом-1см-1, электропроводность указана при комнатной температуре). Стааф Карл Стааф (Staaff) (правильнее Став) Карл (21.1. Целик, часть залежи (пласта) полезного ископаемого, оставляемая нетронутой при разработке месторождения с целью управления кровлей и для охраны горных выработок и наземных сооружений. Байхэ, река в северной части КНР, одна из составляющих р. Гомогамия (от гомо... и греч. gámos — брак), 1) одновременное созревание рыльца и пыльников у обоеполого цветка, благодаря чему возможно самоопыление (ср. Карп, одомашненная форма сазана, разводимая в прудах. Маурандия (Maurandya), род растений семейства норичниковых. Плакорная растительность (от греч. plax — плоскость, равнина), растительность ровных водораздельных пространств (плакоров), сложенных в пределах Европейской части СССР главным образом суглинистыми или глинистыми почвообразующими породами. Сорбоза (от лат. sorbum — рябина), моносахарид из группы кетогексоз. Храбан Мавр, Рабан Мавр [Hrabanus (Rabanus) Maurus] (около 780, Майнц, — 4. Ахроматин (от греч. achroma tos — бесцветный), слабо окрашивающееся красителями вещество клеточного ядра. Гленн Джон Гленн (Glenn) Джон (р. 18.7.1921, Кембридж, штат Огайо), лётчик-космонавт США, подполковник ВМФ. |
|