Лёд
Большая Советская Энциклопедия. Статьи для написания рефератов, курсовых работ, научные статьи, биографии, очерки, аннотации, описания.
|
|
| ЛЁБ |
| ЛЁВ |
| ЛЁГ |
| ЛЁД |
| ЛЁЙ |
| ЛЁЛ |
| ЛЁН |
| ЛЁС |
| ЛЁТ |
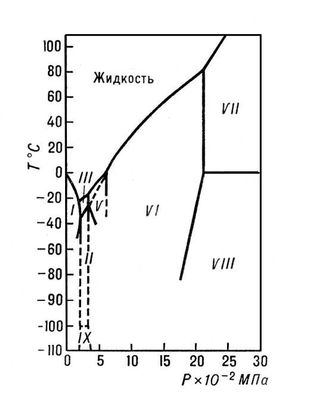
Лёд, вода в твёрдом состоянии; известно 10 кристаллических модификаций Лёд и аморфный Лёд На рис. 1 изображена фазовая диаграмма воды, из которой видно, при каких температурах и давлениях устойчива та или иная модификация. Наиболее изученным является Лёд 1 (табл. 1 и 2) — единственная модификация Лёд, обнаруженная в природе. Лёд встречается в природе в виде собственно Лёд (материкового, плавающего, подземного и т.д.), а также в виде снега, инея и т.д. Природный Лёд обычно значительно чище, чем вода, т.к. растворимость веществ (кроме NH4F) во Лёд крайне плохая. Лёд может содержать механические примеси — твёрдые частицы, капельки концентрированных растворов, пузырьки газа. Наличием кристалликов соли и капелек рассола объясняется солоноватость морского льда. Общие запасы Лёд на Земле около 30 млн. км3. Имеются данные о наличии Лёд на планетах Солнечной системы и в кометах. Основные запасы Лёд на Земле сосредоточены в полярных странах (главным образом в Антарктиде, где толщина слоя Лёд достигает 4 км).
Рис. 1. Фазовая диаграмма воды.
Табл. 1. — Некоторые свойства льда I
|
Свойство |
Значение |
Примечание |
|
Теплоемкость, кал/(г··°C) Теплота таяния, кал/г Теплота парообразования, кал/г |
0,51 (0°C) 79,69 677 |
Сильно уменьшается с понижением температуры |
|
Коэффициент термического расширения, 1/°C |
9,1·10—5 (0°C) |
|
|
Теплопроводность, кал/(см сек··°C) |
4,99·10—3 |
|
|
Показатель преломления: для обыкновенного луча для необыкновенного луча |
1,309 (—3°C) 1,3104 (—3°C) |
|
|
Удельная электрическая проводимость, ом—1·см—1 |
10—9 (0°C) |
Кажущаяся энергия активации 11ккал/моль |
|
Поверхностная электропроводность, ом—1 |
10—10 (—11°C) |
Кажущаяся энергия активации 32ккал/моль |
|
Модуль Юнга, дин/см |
9·1010 (—5°C) |
Поликристаллич. лёд |
|
Сопротивление, Мн/м2 : раздавливанию разрыву срезу |
2,5 1,11 0,57 |
Поликристаллический лёд Поликристаллический лёд Поликристаллический лёд |
|
Средняя эффективная вязкость, пз |
1014 |
Поликристаллический лёд |
|
Показатель степени степенного закона течения |
3 |
|
|
Энергия активации при деформировании и механической релаксации, ккал/моль |
11,44—21,3 |
Линейно растет на 0,0361 ккал/(моль·°C) от 0 до 273,16 К |
Примечание. 1 кал/(г×°С)=4,186 кджl (kг (К); 1 ом-1×см-1=100 сим/м; 1 дин/см=10-3н/м; 1 кал/(см (сек×°С)=418,68 вт/(м (К); 1 пз=10-1 н (сек/м2.
Табл. 2. — Количество, распространение и время жизни льда 1
|
Вид льда |
Масса |
Площадь распространения |
Средняя концен |
Скорость прироста массы, г/год |
Среднее время жизни, год | ||
|
г |
% |
млн. км2 |
% | ||||
|
Ледники |
2,4·1022 |
98,95 |
16,1 |
10,9 суши |
1,48·105 |
2,5·1018 |
9580 |
|
Подземный лёд |
2·1020 |
0,83 |
21 |
14,1 суши |
9,52·103 |
6·1018 |
30—75 |
|
Морской лёд |
3,5·1019 |
0,14 |
26 |
7,2 океана |
1,34·102 |
3,3·1019 |
1,05 |
|
Снежный покров |
1,0·1019 |
0,04 |
72,4 |
14,2 Земли |
14,5 |
2·1019 |
0.3—0,5 |
|
Айсберги |
7,6·1018 |
0,03 |
63,5 |
18,7 океана |
14,3 |
1,9·1018 |
4,07 |
|
Атмосферный лёд |
1,7·1018 |
0,01 |
510,1 |
100 Земли |
3,3·10—1 |
3,9·1020 |
4·10—3 |
В связи с широким распространением воды и Лёд на земной поверхности резкое отличие части свойств Л. от свойств др. веществ играет важную роль в природных процессах. Вследствие меньшей, чем у воды, плотности Лёд образует на поверхности воды плавучий покров, предохраняющий реки и водоёмы от промерзания до дна. Зависимость между установившейся скоростью течения и напряжением у поликристаллического Лёд гиперболическая; при приближённом описании её степенным уравнением показатель степени увеличивается по мере роста напряжения; кроме того, скорость течения прямо пропорциональна энергии активации и обратно пропорциональна абсолютной температуре, так что с понижением температуры Лёд приближается к абсолютно твёрдому телу. В среднем при близкой к таянию температуре текучесть Лёд в 106 раз выше, чем у горных пород. Благодаря текучести Лёд не накопляется беспредельно, а стекает с тех частей земной поверхности, где его выпадает больше, чем стаивает (см. Ледники). Вследствие очень высокой отражательной способности Лёд (0,45) и особенно снега (до 0,95) покрытая ими площадь — в среднем за год около 72 млн. км2 в высоких и средних широтах обоих полушарий — получает солнечного тепла на 65% меньше нормы и является мощным источником охлаждения земной поверхности, чем в значительной мере обусловлена современная широтная климатическая зональность. Летом в полярных областях солнечная радиация больше, чем в экваториальном поясе, тем не менее температура остаётся низкой, т. к. значительная часть поглощаемого тепла затрачивается на таяние Лёд, имеющего очень высокую теплоту таяния.
Лёд II, III и V длительное время сохраняются при атмосферном давлении, если температура не превышает —170°С. При нагревании приблизительно до —150°С они превращаются в кубический Лёд (Лёд Ic), не показанный на диаграмме, т. к. неизвестно, является ли он стабильной фазой. Др. способ получения Лёд Ic — конденсация водяных паров на охлажденную до —120°С подложку. При конденсации паров на более холодной подложке образуется аморфный Лёд Обе эти формы Лёд могут самопроизвольно переходить в гексагональный Лёд I, причём тем скорее, чем выше температура.
Лёд IV является метастабильной фазой в зоне устойчивости Лёд V. Лёд IV легче образуется, а возможно и стабилен, если давлению подвергается тяжёлая вода. Кривая плавления льда VII исследована до давления 20 Гн/м2 (200 тыс. кгс/см2). При этом давлении Лёд VII плавится при температуре 400°С. Лёд VIII является низкотемпературной упорядоченной формой Лёд VII. Лёд IX — метастабильная фаза, возникающая при переохлаждении Лёд III и по существу представляющая собой низкотемпературную его форму. Вообще явления переохлаждения и метастабильные равновесия очень характерны для фаз, образуемых водой. Некоторые из линий метастабильных равновесий обозначены на диаграмме пунктиром.
Полиморфизм Лёд был обнаружен Г. Тамманом (1900) и подробно изучен П. Бриджменом (начиная с 1912). С 60-х гг. фазовая диаграмма воды, полученная Бриджменом, несколько раз дополнялась и уточнялась. В табл. 3 и 4 приведены некоторые данные о структурах модификаций Лёд и некоторые их свойства.
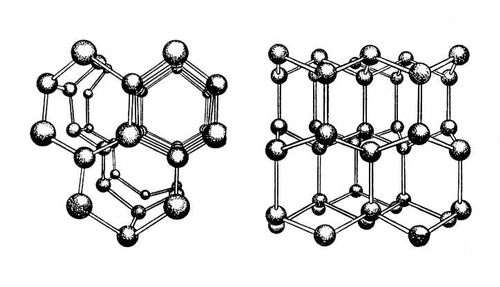
Кристаллы всех модификаций Лёд построены из молекул воды H2O, соединённых водородными связями в трёхмерный каркас (рис. 2). Каждая молекула участвует в 4 таких связях, направленных к вершинам тетраэдра. В структурах Лёд I, Ic, VII и VIII этот тетраэдр правильный, т. е. угол между связями составляет 109°28'. Большая плотность Лёд VII и VIII объясняется тем, что их структуры содержат по 2 трёхмерные сетки водородных связей (каждая из которых идентична структуре Лёд Ic), вставленные одна в другую. В структурах Лёд II, III, V и VI тетраэдры заметно искажены. В структурах Лёд VI, VII и VIII можно выделить 2 взаимоперекрещивающиеся системы водородных связей. Данные о положениях протонов в структурах Лёд менее определенны, чем атомов кислорода. Можно утверждать, что конфигурация молекулы воды, характерная для пара, сохраняется и в твёрдом состоянии (по-видимому, несколько удлиняются расстояния О — Н вследствие образования водородных связей), а протоны тяготеют к линиям, соединяющим центры атомов кислорода. Т. о. возможны 6 более или менее эквивалентных ориентаций молекул воды относительно их соседей. Часть из них исключается, поскольку нахождение одновременно 2 протонов на одной водородной связи маловероятно, но остаётся достаточная неопределённость в ориентации молекул воды. Она осуществляется в большинстве модификаций Лёд — I, III, V, VI и VII (и по-видимому в Ic), так что, по выражению Дж. Бернала, Лёд кристалличен в отношении атомов кислорода и стеклообразен в отношении атомов водорода. Во Лёд II, VIII и IX молекулы воды ориентационно упорядочены.
Рис. 2. Схема структуры льда I (показаны атомы кислорода и направления водородных связей) в двух проекциях.
Табл. 3. — Некоторые данные о структурах модификаций льда
|
Модифи |
Сингония |
Фёдоровская группа |
Длины водородных связей, |
Углы О—О—О в тетраэдрах |
|
I Ic II III V VI VII VIII IX |
Гексагональная Кубическая Тригональная Тетрагональная Моноклинная Тетрагональная Кубическая Кубическая Тетрагональная |
P63/mmc F43m R3 P41212 A2/a P42/nmc Im3m Im3m P41212 |
2,76 2,76 2,75—2,84 2,76—2,8 2,76—2,87 2,79—2,82 2,86 2,86 2,76—2,8 |
109,5 109,5 80—128 87—141 84—135 76—128 109,5 109,5 87—141 |
Примечание. 1 A=10-10 м.
Табл. 4. — Плотность и статическая диэлектрическая проницаемость различных льдов
Модификация |
Темп-ра, °С |
Давление, Мн/м2 |
Плотность, г/см2 |
Диэлектрическая проницаемость |
|
I Ic II III V VI VII VIII IX |
0 —130 —35 —22 —5 15 25 —50 —110 |
0,1 0,1 210 200 530 800 2500 2500 230 |
0,92 0,93 1,18 1,15 1,26 1,34 1,65 1,66 1,16 |
94 — 3,7 117 144 193 ~150 ~3 ~4 |
Лёд в атмосфере, в воде, на земной и водной поверхности и в земной коре оказывает большое влияние на условия обитания и жизнедеятельности растений и животных, на разные виды хозяйственной деятельности человека. Он может вызывать ряд стихийных явлений с вредными и разрушительными последствиями (обледенение летательных аппаратов, судов, сооружений, дорожного полотна и почвы, градобития, метели и снежные заносы, речные заторы и зажоры с наводнениями, ледяные обвалы, разрыв корней растений при образовании слоев Лёд в почве и др.). Прогнозирование, обнаружение, предотвращение вредных явлений, борьба с ними и использование Лёд в различных целях (снегозадержание, устройство ледяных переправ, изотермических складов, облицовка хранилищ, льдозакладка шахт и т.п.) представляют предмет ряда разделов гидрометеорологических и инженерно-технических знаний (ледотехника, снеготехника, инженерное мерзлотоведение и др.), деятельности специальных служб (ледовая разведка, ледокольный транспорт, снегоуборочная техника, искусственное сбрасывание лавин и т.д.). Для некоторых видов спорта используются катки с искусственным охлаждением, позволяющие проводить соревнования на Лёд в тёплое время года и в закрытом помещении. Природный Лёд используется для хранения и охлаждения пищевых продуктов, биологических и медицинских препаратов, для чего он специально производится и заготавливается (см. Ледник, Льдопроизводство).
Лит.: Шумский П. А., Основы структурного ледоведения, М., 1955; Паундер Э. Р., Физика льда, пер. с англ., М., 1967; Eisenberg D., Kauzmann W., The structure and properties of water, Oxf., 1969; Fletcher N. H., The chemical physics of ice, Camb., 1970.
Г. Г. Маленков.
|
Так же Вы можете узнать о... Объектное спряжение, выражение в морфологической форме глагола категорий именного или местоименного объекта (его лица, числа, иногда рода или класса). Пани Марио Пани (Pani) Марио (родился 29.3.1911, Мехико), мексиканский архитектор. Плеве Вячеслав Константинович [1846 — 15 (28). Приусадебный участок, в СССР форма индивидуального землепользования граждан. Реза Аббаси, Ризайе Аббаси (около 1575, Кашан, — 1635), иранский миниатюрист. Самостерильность, неспособность растений к образованию семян при самоопылении. Синтез линейной цепи электрической, определение структуры линейной электрической цепи и параметров элементов, из которых она должна быть собрана, по заданным её свойствам или характеристикам. Сретенск, город, центр ого района Читинской области РСФСР. Танеев Владимир Иванович [24.8(5.9).1840, Владимир, — 21. Треугольник (созвездие) Треугольник (лат. Triangulum), созвездие Северного полушария неба; наиболее яркие звёзды 3,0 и 3,4 визуальной звёздной величины. Фактор (нем. Faktor, от лат. factor – делающий, производящий), причина, движущая сила какого-либо процесса, определяющая его характер или отдельные его черты. Ханты-Мансийский автономный округ (до 1940 — Остяко-Вогульский национальный округ, до 1977 — Ханты-Мансийский национальный округ), в составе Тюменской области РСФСР. Частное определение, в советском процессуальном праве специальное определение суда. Шубиц (Šubic), словенские живописцы, братья. Юрьевка (пос. гор. типа в Ворошиловградской обл.) Юрьевка, посёлок городского типа в Лутугинском районе Ворошиловградской области УССР. Аллануров Хыдыр Алланурович (р. 7.11.1922, г. |
|