Уран (хим. элемент)
Большая Советская Энциклопедия. Статьи для написания рефератов, курсовых работ, научные статьи, биографии, очерки, аннотации, описания.
|
|
| УРА |
| УРБ |
| УРВ |
| УРГ |
| УРД |
| УРЕ |
| УРЖ |
| УРЗ |
| УРИ |
| УРК |
| УРЛ |
| УРМ |
| УРН |
| УРО |
| УРС |
| УРТ |
| УРУ |
| УРФ |
| УРЦ |
| УРШ |
| УРЫ |
| УРЮ |
| УРЯ |
Уран (лат. Uranium), U, радиоактивный химический элемент III группы периодической системы Менделеева, относится к семейству актиноидов, атомный номер 92, атомная масса 238,029; металл. Природный Уран (хим. элемент) состоит из смеси трёх изотопов: 238U – 99,2739% с периодом полураспада T1/2 = 4,51·109 лет, 235U – 0,7024% (T1/2 = 7,13·108 лет) и 234U – 0,0057% (T1/2 = 2,48·105 лет). Из 11 искусственных радиоактивных изотопов с массовыми числами от 227 до 240 долгоживущий – 233U (T1/2 = 1,62·105лет); он получается при нейтронном облучении тория. 238U и 235U являются родоначальниками двух радиоактивных рядов.
Историческая справка. Уран (хим. элемент) открыт в 1789 нем. химиком М. Г. Клапротом и назван им в честь планеты Уран, открытой В. Гершелем в 1781. В металлическом состоянии Уран (хим. элемент) получен в 1841 франц. химиком Э. Пелиго при восстановлении UCl4 металлическим калием. Первоначально Уран (хим. элемент) приписывали атомную массу 120, и только в 1871 Д. И. Менделеев пришёл к выводу, что эту величину надо удвоить.
Длительное время уран представлял интерес только для узкого круга химиков и находил ограниченное применение для производства красок и стекла. С открытием явления радиоактивности Уран (хим. элемент) в 1896 и радия в 1898 началась промышленная переработка урановых руд с целью извлечения и использования радия в научных исследованиях и медицине. С 1942, после открытия в 1939 явления деления ядер (см. Ядра атомного деление), Уран (хим. элемент) стал основным ядерным топливом.
Распространение в природе. Уран (хим. элемент) – характерный элемент для гранитного слоя и осадочной оболочки земной коры. Среднее содержание Уран (хим. элемент) в земной коре (кларк) 2,5·10-4% по массе, в кислых изверженных породах 3,5·10-4%, в глинах и сланцах 3,2·10-4%, в основных породах 5·10-5%, в ультраосновных породах мантии 3·10-7%. Уран (хим. элемент) энергично мигрирует в холодных и горячих, нейтральных и щелочных водах в форме простых и комплексных ионов, особенно в форме карбонатных комплексов. Важную роль в геохимии Уран (хим. элемент) играют окислительно-восстановительные реакции, поскольку соединения Уран (хим. элемент), как правило, хорошо растворимы в водах с окислительной средой и плохо растворимы в водах с восстановительной средой (например, сероводородных).
Известно около 100 минералов Уран (хим. элемент); промышленное значение имеют 12 из них (см. Урановые руды). В ходе геологической истории содержание Уран (хим. элемент) в земной коре уменьшилось за счёт радиоактивного распада; с этим процессом связано накопление в земной коре атомов РЬ, Не. Радиоактивный распад Уран (хим. элемент) играет важную роль в энергетике земной коры, являясь существенным источником глубинного тепла.
Физические свойства. Уран (хим. элемент) по цвету похож на сталь, легко поддаётся обработке. Имеет три аллотропические модификации – a, b и g с температурами фазовых превращений: a®b 668,8±0,4°C, b® g 772,2 ± 0,4 °С; a-форма имеет ромбическую решётку a = 2.8538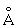 , b = 5,8662
, b = 5,8662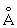 , с = 4,9557
, с = 4,9557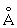 ), b-форма – тетрагональую решётку (при 720 °С а = 10,759
), b-форма – тетрагональую решётку (при 720 °С а = 10,759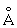 , b = 5,656
, b = 5,656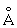 ), g-форма – объёмноцентрированную кубическую решётку (при 850°C а = 3,538
), g-форма – объёмноцентрированную кубическую решётку (при 850°C а = 3,538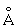 ). Плотность Уран (хим. элемент) в a-форме (25°C) 19,05 ± 0,2 г/см3, tпл 1132 ± 1°С; tkип 3818 °С; теплопроводность (100–200°C), 28,05 вт/(м·К) [0,067 кал/(см·сек·°С)], (200–400 °C) 29,72 вт/(м·К) [0,071 кал/(см·сек·°С)]; удельная теплоёмкость (25°C) 27,67 кдж/(кг·К) [6,612 кал/(г·°С)]; удельное электросопротивление при комнатной температуре около 3·10-7ом·см, при 600°C 5,5·10-7 ом·см; обладает сверхпроводимостью при 0,68 ± 0,02К; слабый парамагнетик, удельная магнитная восприимчивость при комнатной температуре 1,72·10-6.
). Плотность Уран (хим. элемент) в a-форме (25°C) 19,05 ± 0,2 г/см3, tпл 1132 ± 1°С; tkип 3818 °С; теплопроводность (100–200°C), 28,05 вт/(м·К) [0,067 кал/(см·сек·°С)], (200–400 °C) 29,72 вт/(м·К) [0,071 кал/(см·сек·°С)]; удельная теплоёмкость (25°C) 27,67 кдж/(кг·К) [6,612 кал/(г·°С)]; удельное электросопротивление при комнатной температуре около 3·10-7ом·см, при 600°C 5,5·10-7 ом·см; обладает сверхпроводимостью при 0,68 ± 0,02К; слабый парамагнетик, удельная магнитная восприимчивость при комнатной температуре 1,72·10-6.
Механические свойства Уран (хим. элемент) зависят от его чистоты, от режимов механической и термической обработки. Среднее значение модуля упругости для литого Уран (хим. элемент) 20,5·10-2Мн/м2 [20,9·10-3кгс/мм2] предел прочности при растяжении при комнатной температуре 372–470 Мн/м2 [38–48 кгс/мм2], прочность повышается после закалки из bи g-фаз; средняя твёрдость по Бринеллю 19,6–21,6·102Мн/м2 [200–220 кгс/мм2].
Облучение потоком нейтронов (которое имеет место в ядерном реакторе) изменяет физико-механические свойства Уран (хим. элемент): развивается ползучесть и повышается хрупкость, наблюдается деформация изделий, что заставляет использовать Уран (хим. элемент) в ядерных реакторах в виде различных урановых сплавов.
Уран (хим. элемент) – радиоактивный элемент. Ядра 235U и 233U делятся спонтанно, а также при захвате как медленных (тепловых), так и быстрых нейтронов с эффективным сечением деления 508·10-24 см2 (508 барн) и 533·10-24 см2 (533 барн) соответственно. Ядра 238U делятся при захвате только быстрых нейтронов с энергией не менее 1 Мэв; при захвате медленных нейтронов 238U превращается в 239Pu, ядерные свойства которого близки к 235U. Критич. масса Уран (хим. элемент) (93,5% 235U) в водных растворах составляет менее 1 кг, для открытого шара – около 50 кг, для шара с отражателем – 15 – 23 кг; критическая масса 233U – примерно 1/3 критической массы 235U.
Химические свойства. Конфигурация внешней электронной оболочки атома Уран (хим. элемент) 7s26d15f3. Уран (хим. элемент) относится к реакционноспособным металлам, в соединениях проявляет степени окисления + 3, + 4, + 5, + 6, иногда + 2; наиболее устойчивы соединения U (IV) и U (VI). На воздухе медленно окисляется с образованием на поверхности плёнки двуокиси, которая не предохраняет металл от дальнейшего окисления. В порошкообразном состоянии Уран (хим. элемент) пирофорен и горит ярким пламенем. С кислородом образует двуокись UO2, трёхокись UO3 и большое число промежуточных окислов, важнейший из которых U3O8. Эти промежуточные окислы по свойствам близки к UO2 и UO3. При высоких температурах UO2 имеет широкую область гомогенности от UO1,60 до UO2,27. С фтором при 500–600°C образует тетрафторидирд (зелёные игольчатые кристаллы, малорастворимые в воде и кислотах) и гексафторид UF6 (белое кристаллическое вещество, возгоняющееся без плавления при 56,4°C); с серой – ряд соединений, из которых наибольшее значение имеет US (ядерное горючее). При взаимодействии Уран (хим. элемент) с водородом при 220 °С получается гидрид UH3; с азотом при температуре от 450 до 700 °С и атмосферном давлении – нитрид U4N7, при более высоком давлении азота и той же температуре можно получить UN, U2N3 и UN2; с углеродом при 750–800°C – монокарбид UC, дикарбид UC2, а также U2C3; с металлами образует сплавы различных типов (см. Урановые сплавы). Уран (хим. элемент) медленно реагирует с кипящей водой с образованием UO2 и H2, с водяным паром – в интервале температур 150–250 °С; растворяется в соляной и азотной кислотах, слабо – в концентрированной плавиковой кислоте. Для U (VI) характерно образование иона уранила UO22 +; соли уранила окрашены в жёлтый цвет и хорошо растворимы в воде и минеральных кислотах; соли U (IV) окрашены в зелёный цвет и менее растворимы; ион уранила чрезвычайно способен к комплексообразованию в водных растворах как с неорганическими, так и с органическими веществами; наиболее важны для технологии карбонатные, сульфатные, фторидные, фосфатные и др. комплексы. Известно большое число уранатов (солей не выделенной в чистом виде урановой кислоты), состав которых меняется в зависимости от условий получения; все уранаты имеют низкую растворимость в воде.
Уран (хим. элемент) и его соединения радиационно и химически токсичны. Предельно допустимая доза (ПДД) при профессиональном облучении 5 бэр в год.
Получение. Уран (хим. элемент) получают из урановых руд, содержащих 0,05–0,5% U. Руды практически не обогащаются, за исключением ограниченного способа радиометрической сортировки, основанной на излучении радия, всегда сопутствующего урану. В основном руды выщелачивают растворами серной, иногда азотной кислот или растворами соды с переводом Уран (хим. элемент) в кислый раствор в виде UO2SO4 или комплексных анионов [UO2(SO4)3]4-, а в содовый раствор – в виде [UO2(CO3)3]4-. Для извлечения и концентрирования Уран (хим. элемент) из растворов и пульп, а также для очистки от примесей применяют сорбцию на ионообменных смолах и экстракцию органическими растворителями (трибутилфосфат, алкилфосфорные кислоты, амины). Далее из растворов добавлением щёлочи осаждают уранаты аммония или натрия или гидроокись U (OH)4. Для получения соединений высокой степени чистоты технические продукты растворяют в азотной кислоте и подвергают аффинажным операциям очистки, конечными продуктами которых являются UO3 или U3O8; эти окислы при 650–800°C восстанавливаются водородом или диссоциированным аммиаком до UO2 с последующим переводом его в UF4 обработкой газообразным фтористым водородом при 500–600°C. UF4 может быть получен также при осаждении кристаллогидрата UF4·nH2O плавиковой кислотой из растворов с последующим обезвоживанием продукта при 450°C в токе водорода. В промышленности основным способом получения Уран (хим. элемент) из UF4 является его кальциетермическое или магниетермическое восстановление с выходом Уран (хим. элемент) в виде слитков массой до 1,5 т. Слитки рафинируются в вакуумных печах.
Очень важным процессом в технологии Уран (хим. элемент) является обогащение его изотопом 235U выше естественного содержания в рудах или выделение этого изотопа в чистом виде (см. Изотопов разделение), поскольку именно 235U – основное ядерное горючее; осуществляется это методами газовой термодиффузии, центробежными и др. методами, основанными на различии масс 235U и 238U; в процессах разделения Уран (хим. элемент) используется в виде летучего гексафторида UF6. При получении Уран (хим. элемент) высокой степени обогащения или изотопов учитываются их критические массы; наиболее удобный способ в этом случае – восстановление окислов Уран (хим. элемент) кальцием; образующийся при этом шлак CaO легко отделяется от Уран (хим. элемент) растворением в кислотах.
Для получения порошкообразного Уран (хим. элемент), двуокиси, карбидов, нитридов и др. тугоплавких соединений применяются методы порошковой металлургии.
Применение. Металлический Уран (хим. элемент) или его соединения используются в основном в качестве ядерного горючего в ядерных реакторах. Природная или малообогащённая смесь изотопов Уран (хим. элемент) применяется в стационарных реакторах атомных электростанций, продукт высокой степени обогащения – в ядерных силовых установках или в реакторах, работающих на быстрых нейтронах. 235U является источником ядерной энергии в ядерном оружии. 238U служит источником вторичного ядерного горючего – плутония.
В. М. Кулифеев.
Уран в организме. В микроколичествах (10-5–10-5%) обнаруживается в тканях растений, животных и человека. В золе растений (при содержании Уран (хим. элемент) в почве около·10-4) его концентрация составляет 1,5·10-5%. В наибольшей степени Уран (хим. элемент) накапливается некоторыми грибами и водорослями (последние активно участвуют в биогенной миграции Уран (хим. элемент) по цепи вода – водные растения – рыба – человек). В организм животных и человека Уран (хим. элемент) поступает с пищей и водой в желудочно-кишечный тракт, с воздухом в дыхательные пути, а также через кожные покровы и слизистые оболочки. Соединения Уран (хим. элемент) всасываются в желудочно-кишечном тракте – около 1% от поступающего количества растворимых соединений и не более 0,1% труднорастворимых; в лёгких всасываются соответственно 50% и 20%. Распределяется Уран (хим. элемент) в организме неравномерно. Основные депо (места отложения и накопления) – селезёнка, почки, скелет, печень и, при вдыхании труднорастворимых соединений, – лёгкие и бронхо-лёгочные лимфатические узлы. В крови Уран (хим. элемент) (в виде карбонатов и комплексов с белками) длительно не циркулирует. Содержание Уран (хим. элемент) в органах и тканях животных и человека не превышает 10-7г/г. Так, кровь крупного рогатого скота содержит 1·10-8г/мл, печень 8·10-8г/г, мышцы 4·10-8г/г, селезёнка 9·10-8г/г. Содержание Уран (хим. элемент) в органах человека составляет: в печени 6·10-9г/г, в лёгких 6·10-9–9·10-9г/г, в селезёнке 4,7·10-9г/г, в крови 4·10-9г/мл, в почках 5,3·10-9 (корковый слой) и 1,3·10-9г/г (мозговой слой), в костях 1·10-9г/г, в костном мозге 1·10-9г/г, в волосах 1,3·10-7г/г. Уран (хим. элемент), содержащийся в костной ткани, обусловливает её постоянное облучение (период полувыведения Уран (хим. элемент) из скелета около 300 сут). Наименьшие концентрации Уран (хим. элемент) – в головном мозге и сердце (10-10г/г). Суточное поступление Уран (хим. элемент) с пищей и жидкостями – 1,9·10-6г, с воздухом – 7·10-9г. Суточное выведение Уран (хим. элемент) из организма человека составляет: с мочой 0,5·10-7–5·10-7, с калом – 1,4·10-6–1,8·10-6г, с волосами – 2·10-8г.
По данным Международной комиссии по радиационной защите, среднее содержание Уран (хим. элемент) в организме человека 9·10-8 г. Эта величина для различных районов может варьировать. Полагают, что Уран (хим. элемент) необходим для нормальной жизнедеятельности животных и растений, однако его физиологические функции не выяснены.
Г. П. Галибин.
Токсическоедействие Уран (хим. элемент) обусловлено его химическими свойствами и зависит от растворимости: более токсичны уранил и др. растворимые соединения Уран (хим. элемент) Отравления Уран (хим. элемент) и его соединениями возможны на предприятиях по добыче и переработке уранового сырья и др. промышленных объектах, где он используется в технологическом процессе. При попадании в организм Уран (хим. элемент) действует на все органы и ткани, являясь общеклеточным ядом. Признаки отравления обусловлены преим. поражением почек (появление белка и сахара в моче, последующая олигурия), поражаются также печень и желудочно-кишечный тракт. Различают острые и хронические отравления; последние характеризуются постепенным развитием и меньшей выраженностью симптомов. При хронической интоксикации возможны нарушения кроветворения, нервной системы и др. Полагают, что молекулярный механизм действия Уран (хим. элемент) связан с его способностью подавлять активность ферментов.
Профилактика отравлений: непрерывность технологических процессов, использование герметичной аппаратуры, предупреждение загрязнения воздушной среды, очистка сточных вод перед спуском их в водоёмы, мед. контроль за состоянием здоровья рабочих, за соблюдением гигиенических нормативов допустимого содержания Уран (хим. элемент) и его соединений в окружающей среде.
В. Ф. Кириллов.
Лит.: Учение о радиоактивности. История и современность, под ред. Б. М. Кедрова, М., 1973; Петросьянц А. М., От научного поиска к атомной промышленности, М., 1970; Емельянов В. С., Евстюхин А. И., Металлургия ядерного горючего, М., 1964; Сокурский Ю. Н., Стерлин Я. М., Федорченко В. А., Уран и его сплавы, М., 1971; Евсеева Л. С., Перельман А. И., Иванов К. Е., Геохимия урана в зоне гнпергениза, 2 изд., М., 1974; Фармакология и токсикология урановых соединений, [пер. с англ.], т. 2, М., 1951; Гуськова В. Н., Уран. Радиационно-гигиеническая характеристика, М., 1972; Андреева О. С., Гигиена труда при работе с ураном и его соединениями, М., 1960; Новиков Ю. В,, Гигиенические вопросы изучения содержания урана во внешней среде и его влияния на организм, М., 1974.
|
Так же Вы можете узнать о... Посадочная крепь, индивидуальная крепь очистных выработок, предназначенная для управления кровлей методом обрушения (посадки) кровли. Сейсмическая шкала, шкала для оценки интенсивности колебаний на поверхности Земли при землетрясениях. Теплоизоляция, тепловая изоляция, термоизоляция, защита зданий, тепловых промышленных установок (или отдельных их узлов), холодильных камер, трубопроводов и прочего от нежелательного теплового обмена с окружающей средой. Хёугесунн (Haugesund), город в Норвегии, в фюльке Ругаланн, порт на берегу Северного моря 27 тыс. Юшневский Алексей Петрович [12(23).3.1786, Подольская губерния, — 10(22). Беккари яма, что биотермическая яма. Время жизни в физике, средняя продолжительность τ существования: 1) возбуждённых состояний атомов и молекул, заканчивающегося спонтанным (самопроизвольным) переходом частиц в менее возбуждённое или в основное (невозбуждённое) состояние; В. Диализ (от греч. dialysis — разложение, отделение), удаление из коллоидных систем и растворов высокомолекулярных соединений примесей низкомолекулярных веществ с помощью полупроницаемых мембран, т. Калина (Viburnum), род большей частью листопадных кустарников или небольших деревьев семейства жимолостных. Ксенофан Колофонский (Xenophánēs) (6—5 вв. Метатеория (от мета...), теория, анализирующая структуру, методы и свойства какой-либо другой теории — т. Орегонский договор 1846, договор между США и Великобританией от 15 июня 1846, положивший конец их конфликту по вопросу об Орегоне (области, простиравшейся от Скалистых гор до Тихого океана между 42° и 54°40' северной широты и формально, согласно англо-американскому договору 1818, находившейся в совместном владении США и Великобритании). Псевдопериптер (от псевдо... и периптер), тип античного храма. Скляренко Семен Дмитриевич [13(26).9.1901, с. Третьяковская галерея в Москве, крупнейший музей русского и советского искусства. Циньхуандао, город в Северном Китае, в провинции Хэбэй. Азовское сидение, героическая оборона Азова донскими казаками в 1637—42. Боевые традиции, военные традиции, исторически сложившиеся в армии и на флоте правила, обычаи и нормы поведения военнослужащих в мирное и военное время. |
|